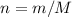 .
. 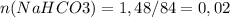 моль.
моль.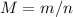 . M (CnH2nO2)=2.44/0.02=122 г/моль.
. M (CnH2nO2)=2.44/0.02=122 г/моль.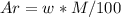 . Ar (C)=68.85*122/100=84. Найдем, сколько атомов углерода входит в соединение, разделив на атомную массу одного углерода: 84/12=7. Тогда, формула кислоты будет иметь вид: C7H14O2. Рассчитаем молекулярную массу полученной кислоты: 12*7(C)+14*1(H)+16*2(O)=130 г/моль. Получается, что 8 атомов водорода лишние (130-122=8).
. Ar (C)=68.85*122/100=84. Найдем, сколько атомов углерода входит в соединение, разделив на атомную массу одного углерода: 84/12=7. Тогда, формула кислоты будет иметь вид: C7H14O2. Рассчитаем молекулярную массу полученной кислоты: 12*7(C)+14*1(H)+16*2(O)=130 г/моль. Получается, что 8 атомов водорода лишние (130-122=8).
В пределах периода число энергетических уровней у атомов химических элементов "9) не изменяется", а вот радиус "6) уменьшается". В периодической системе элементы расположены по группам и периодам. Общее количество электронов в атоме равно "4) порядковому номеру элемента". Номер периода соответствует "7) количеству энергетических уровней". Номер группы показывает "2) число электронов на внешнем уровне элементов главных подгрупп". Завершенный внешний уровень содержит "5) восемь электронов". Заряженные частицы, в которые превратились атомы в результате отдачи или присоединения электронов - "10) ионы". Ионная химическая связь образуется между "1) атомами химического элемента-неметалла и металла" или "11) ионами". Заряд иона определяется количеством "8) отданных или принятых электронов".