CuCl2 + 2NaOH = Cu(OH)2(стрелка вниз, нерастворим) + 2NaCl
Cu(2+) + 2Cl(-) + 2Na(+) + 2OH(-) = Cu(OH)2(стрелка вниз , нерастворим) + 2Na(+) + 2Cl(-)
Cu(2+) + 2OH(-) = Cu(OH)2(стрелка вниз , нерастворим)
Ca(NO3)2 + Na2CO3 = CaCO3(стрелка вниз, нерастворим) + 2NaNO3
Ca(2+) + 2NO3(-) + 2Na(+) + CO3(2-) = CaCO3 (стрелка вниз, нерастворим) + 2Na(+) + 2NO3(-)
Ca(2+) + CO3(2-) = CaCO3 (стрелка вниз, нерастворим)
AlCl3 + 3AgNO3 = Al(NO3)3 + 3AgCl(стрелка вниз, нерастворим)
Al(3+) + 3Cl(-) + 3Ag(+) + 3NO3(-) = Al(3+) + 3NO3(-) + 3AgCl (стрелка вниз, нерастворим)
3Cl(-) + 3Ag(+) = 3AgCl (стрелка вниз, нерастворим)
Объяснение:
в скобках степени окисления я пишу, степени окисления нужно писать сверху
Рассмотрим поочереди все реакции.
1) 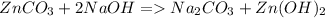
Реакция идет потому что в ходе нее образуется слабый электролит - гидроксид цинка, но углекислого газа не выделяется, так как в растворе присутствует стабильный ион 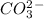 .
.
2) 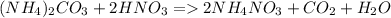
В этой реакции происходит выделение углекислого газа, поскольку 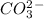 связивается с протонами
связивается с протонами 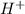 , образуя нустойчивое соединение - угольную кислоту, которая разлагается на углекислый газ и воду.
, образуя нустойчивое соединение - угольную кислоту, которая разлагается на углекислый газ и воду.
3) 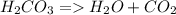
Эта реакция является иллюстрацией предыдущего процесса. Равновесие здесь смещено в сторону образования продуктов, это смещение усиливается еще больше при нагревании.
4) 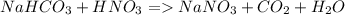
Реакция аналогична пункту 2.
пзгзжгжазгмхожож
Объяснение:
гзшхоэжожсшхз