
1-3
2-4
3 - 4
4-2
5 ( хлороводородная кислота - НЕ ---4
6-1
7-3,5
8- а-1,б-3,в-4
9 2Ca + O2 => 2CaO
CaO + H2O => Ca(OH)2
3Ca(OH)2 + 2H3PO4 => Ca3(PO4)2 + 6H2O
10.
Al2O3 + 3H2SO4 => Al2(SO4)3 + 3H2O
m 40,8г
- находим n (Al2O3) = = = 0,4 моль
M 102г/моль
по уравнению n оксида = n соли
находим массу соли = n * M = 0,4 моль * 342г/моль = 136,8г
Объяснение:
Неметалл водород, а точнее, окислительно-восстановительная пара 2H⁺/H₂ при стандартных условиях имеет (принято) стандартный электродный потенциал = 0 В. При нахождении металла до водорода в ряду активности, потенциал металла ниже (<0 B), в таком случае металл вытеснить водород из кислот. Если металл стои́т в ряду активности после водорода, его потенциал выше (>0 B), такие металлы водород из кислот не вытесняют. Водород появился в ряду активности металлов, потому что относительно стандартного водородного электрода измеряют потенциалы металлов (да и других окислительно-восстановительных пар). Приведём оба примера.
① Zn + 2H⁺ ⟹ Zn²⁺ + H₂↑
анод (–): Zn⁰ ⟶ Zn²⁺ + 2ē (окисление)
катод (+): 2H⁺ + 2ē ⟶ H₂⁰ (восстановление)
ЭДС⁰ = E⁰(2H⁺/H₂) – E⁰(Zn²⁺/Zn) = 0 В – (–0,76 В) = 0,76 В > 0
при положительном значении электродвижущей силы ОВР протекает прямая реакция.
② 2Ag + 2H⁺ ⟸ 2Ag⁺ + H₂↑
анод (предположительно) (–): Ag⁰ ⟶ Ag⁺ + ē (окисление)
катод (предположительно) (+): 2H⁺ + 2ē ⟶ H₂⁰ (восстановление)
ЭДС⁰ = E⁰(2H⁺/H₂) – E⁰(Ag⁺/Ag) = 0 В – 0,8 В = – 0,8 В < 0
при отрицательном значении ЭДС прямая реакция невозможна, протекает обратная реакция.
Таким образом, водород вытесняют металлы, стоящие в ряду активности до самого водорода. А сам водород восстановить металлы из растворов солей, если металл стои́т в ряду напряжений после водорода. Электроотрицательность здесь ни при чём.
Для последнего не до конца уверена, какая первая буква первого элемента, это может быть как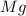 (магний), так и
(магний), так и 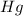 (ртуть), на всякий случай сделаю для обоих.
(ртуть), на всякий случай сделаю для обоих.
Выберите из этих, какой там конкретно.