0 0 +1 -1
1)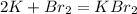
0 +1
K -1e = K |2|восстановитель(окисление)
0 -1
Br2 + 2e = 2Br |1|окислитель(восстановление)
0 0 +2 -3
2)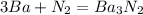
0 +2
Ba - 2e = Ba |3|восстановитель(окисление)
0 -3
N2 + 6e = 2N |1|окислитель(восстановление)
0 +1 +2 0
3)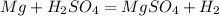
0 +2
Mg -2e = Mg |1|восстановитель(окисление)
+1 0
2H +2e = H2 |1|окислитель(восстановление)
0 +1 +1 0
4)
0 +1
Li - 1e = Li |2|восстановитель(окисление)
+1 0
2H + 2e = H2 |1|окислитель(восстановление)
0 0 +1 -1
1)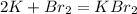
0 +1
K -1e = K |2|восстановитель(окисление)
0 -1
Br2 + 2e = 2Br |1|окислитель(восстановление)
0 0 +2 -3
2)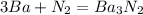
0 +2
Ba - 2e = Ba |3|восстановитель(окисление)
0 -3
N2 + 6e = 2N |1|окислитель(восстановление)
0 +1 +2 0
3)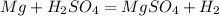
0 +2
Mg -2e = Mg |1|восстановитель(окисление)
+1 0
2H +2e = H2 |1|окислитель(восстановление)
0 +1 +1 0
4)
0 +1
Li - 1e = Li |2|восстановитель(окисление)
+1 0
2H + 2e = H2 |1|окислитель(восстановление)
физические:
- пластичность - изменение формы , железный гвоздь расплющивается при ударе молотком
- плавление
при высокой темепературе железа из твердого становится жидким
химические
железо помещенное в раствор медного купороса покрывается медью
Fe + CuSO4 = FeSO4 + Cu
при наревании железо покрывается черным налетом
4Fe + 3O2 = 2Fe2O3