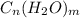 . То есть состоят из углерода и молекул воды, объединенных в одну цельную молекулу. Вообще можно про них долго рассказывать, но если вкратце, то их классификация состоит из того, что они делятся на простые и сложные углеводы. То есть всякие моносахариды (1), дисахариды(2), олигосахариды (до 10) и полисахариды (n). самый известный углевод - глюкоза. Вместе с ним можно взять фруктозу и прочее. Также бывают мальтоза, лактоза, сахароза и тд и тп. К полисахаридам можно отнести крахмал и целлюлозу (из самых известных). Крахмал содержится в животных клетках, а целлюлоза входит в состав клеточной стенки растения
. То есть состоят из углерода и молекул воды, объединенных в одну цельную молекулу. Вообще можно про них долго рассказывать, но если вкратце, то их классификация состоит из того, что они делятся на простые и сложные углеводы. То есть всякие моносахариды (1), дисахариды(2), олигосахариды (до 10) и полисахариды (n). самый известный углевод - глюкоза. Вместе с ним можно взять фруктозу и прочее. Также бывают мальтоза, лактоза, сахароза и тд и тп. К полисахаридам можно отнести крахмал и целлюлозу (из самых известных). Крахмал содержится в животных клетках, а целлюлоза входит в состав клеточной стенки растения
Відповідь:
Пояснення:
одноатомные спирты - ОН гидроксильная
многоатомные спирты - n *ОН гидроксильная
фенолы - ОН гидроксильная, связанная с бензольным кольцом
альдегиды - СОН - карбонильная