Дано:
mр-ра(NaOH) = 100г.
W (NaOH) = 5%
Найти:
m(Cu(OH)2) - ?
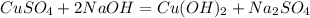
Выпал осадок 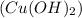
1) mчист.в-ва(NaOH) = mр-ра(NaOH) * W(NaOH) / 100% = 100г. * 5% / 100% = 5г.;
2) n(NaOH) = mчист.в-ва(NaOH) / M(NaOH) = 5г. / 40 г/моль = 0,125 моль;
3) По уравнению n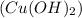 = n(NaOH) / 2 = 0,125 моль / 2 = 0,0625;
= n(NaOH) / 2 = 0,125 моль / 2 = 0,0625;
4) m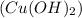 = n
= n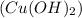 * M
* M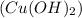 = 0,0625 * 97 г/моль = 6,0625 г.
= 0,0625 * 97 г/моль = 6,0625 г.
ответ: m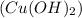 = 6,0625 г.
= 6,0625 г.
Абсолютно уверен, что у меня решено верно! Это задача простая! Никакого избытка с недостатком нет!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
N2 может быть и окислителем и восстановителем, т.к. в состоянии N2 у него степень окисления 0 (промежуточная) например: N2+Li=Li3N здесь N окислил Li, а вот здесь: N2+O2=2NO азот восстановил кислород.
KClO4 - только окислитель, т.к. это сильная кислота, да и хлор в максимальной степени окисления +7. Если в веществе есть элемент с высшей степенью окисления, то он может быть только окислителем.
HBr - один из важнейших восстановителей, как и HCl и HI галогены в этих кислотах имеют низшую степень окисления -1. Вещества в состав которых входят элементы с низшей степенью окисления могут быть только восстановителями.