1)г);
2)б);
3)а).
Объяснение:
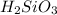
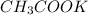

Для начала запишем формулы веществ:⤴.
И нам нужно узнать количество вещества:
чтобы его узнать нам нужно:
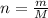
*где m-масса вещества;
*где M-молярная масса.
Массу поделить на Молярную массу.Нам уже известна масса каждых веществ-20 грамм.И поэтому сейчас расчитаем молярную массу.Чтобы её расчитать,нужно сложить все атомные массы веществ.
И у нас получаются такие числа:78,99,171.
Делим их на известные массы:
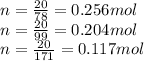
И таким образом,мы узнали количество вещества в разных веществах по 20 грамм.
Дано:
V = 10 л;
T = 27 °C;
n = 1 моль.
Найти:
p — ?
СИ:
27 °C = 300 К.
Задачу решаем по формуле Менделеева-Клапейрона.
‣ pV = nRT; где: p - давление (Па), V - объём (л), n - количество вещества (моль), R - молярная газовая постоянная, равная 8,31 Дж ÷ (моль · К), T - температура (К).
Выражаем давление и подставляем значения.
p = nRT ÷ V = ( 1 моль · 8,31 Дж ÷ (моль · К) · 300 К ) ÷ 10 л = 249,3 (Па).
249,3 Па = 0,2493 кПа.
10⁵ Па = 1 атм ⇒ 249,3 Па = 0,002493 атм.
133,3 Па = 1 мм.рт.ст. ⇒ 249,3 Па ≈ 1,87 мм.рт.ст.
ответ: 0,2493 кПа; 0,002493 атм; 1,87 мм.рт.ст.