Объяснение:
n(H2S) = V(H2S) / Vm = 16,8 л / 22,4 л/моль =0,75 моль
m(H2S) = n * M = 0,75 моль * 34 г/моль =25,5 г
8,5 г х г
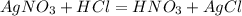
170 г 143,5 г
1. Найдем теоретически возможную массу осадка:
при взаимодействии 170 г нитрата выпадает 143,5 г хлорида, а
при -- // -- 8,5 г_________________х г, откуда
х=8,5*143,5/170=7,18 г
2. Выход продукта - это отношение практической массы продукта реакции(дана по условию задачи и составляет 7 г) к теоретически возможной :
выход продукта=m практическая(AgCl)/m теоретическая(AgCl)=7/7,18=0,97 или 97%
Вот решение:
Дано:
V(смеси) = 150л
W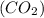 = 15%
= 15%
Найти:
В данной смеси:
V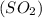 - ?
- ?
V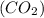 - ?
- ?
Друг, здесь чистая математика:
1) Поскольку объёмная доля последнего составляет 15%, т.е W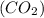 = 15%, найдём сколько литров
= 15%, найдём сколько литров 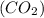 находится в данной смеси:
находится в данной смеси:
Значит, всего 150л-это 100%. Обозначим за x- неизвестный объём 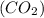 , значит xл- это 15%. Составим пропорцию:
, значит xл- это 15%. Составим пропорцию:
150л-100%
xл-15% => xл=15% * 150л / 100%= 22,5л.;
2) Дальше, мы знаем, что у нас 22,5 л. 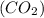 , т.е V
, т.е V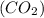 = 22,5л находится в смеси объёмом 150л, а значит объём
= 22,5л находится в смеси объёмом 150л, а значит объём 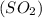 будет равен: 150л-22,5л=127,5л, т.е V
будет равен: 150л-22,5л=127,5л, т.е V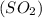 = 127,5л. Всё!
= 127,5л. Всё!
ответ: V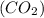 = 22,5л; V
= 22,5л; V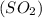 = 127,5л.
= 127,5л.
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Тык
11.2 л. отметь лучшим ответом