РЕШИТЕ Я ВПЕРВЫЕ ЗАДАЮ ВОПРОС МОЖЕТЕ РЕШИТЬ ПРЯМО В ФАЙЛЕ И ПРИСЛАТЬ ТАК БУДЕТ УДОБНЕЕ Практическая работа № 3 Тема: Получение и свойства водорода.Цель: научниться получать водород в лаборатории и изучить его свойства.Оборудование: лабораторный штатив с лапкой, держатель для пробирок, штатив для пробирок, спиртовка, спички. Вещества: гранулы цинка, соляная кислота (разб.) НСl, серная кислота H2SO4 Ход Что делали Что наблюдали Выводы 1. Получение водорода и его собирания методом вытеснения воды В пробирку насыпали несколько гранул цинка. Добавили 2-3 мл соляной кислоты (НСl). Собира- ем газ методов вытеснения воды По мере выделения водорода ко-личество воды в пробирке …… + НСl = …… + …… 2. Получение водорода и его собирания методом вытеснения воздуха Повторили предыдущий опыт только с серной кислотой Н2SО4 Водород собрали в пробирку перевернутую вверх дном ….. + Н2SО4 = …… + ….. 3. Горение водорода Проверить водород на чистоту. Использовали метод горение водорода в пламени спиртовки Спокойное горение водорода с характерным звуком ….. + ….. = Н2О
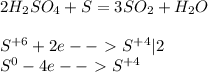
1)Уравнение реакции в общем виде: 4Ме + 3О2 = 2Ме2О3 Отношение количества вещества (Ме) к количеству вещества (Ме2О3) по уравнению реакции =4:2 или 2:1,следовательно (ню) Ме в 2 раза больше, чем Ме2О3. 2)Обозначим М (молярную массу Ме) через Х, тогда М (молярная масса оксида Ме2О3) будет равна 2Х +48 3)количество вещества Ме= м (масса 3г) / м (молярн. масса Х) = 3 / Х г/моль (а) количество вещества оксида = м (5,67г ) / М (2Х +48) =5,67 / 2х+48 г/моль (б) 4)Тогда, т. к. количество вещества Ме в 2 раза больше, следовательно, если значение (а) разделим на (б) = 2 3 / Х : (деление) 5,67 / 2Х +48 =2 3(2Х +48) :( 2Х ) х 5,67=2 6Х +144=11,34Х Х=27(г/моль) т. к. (Х) -молярная масса неизвестного металла, следовательно, это металл Аl(алюминий, степень окисления в оксиде у алюминия (+3),М =27 г моль.