Для указанной реакции при стандартных условиях вычислить: изменение энтальпии, изменение энтропии, изменение изобарно-изотермического потенциала и сделать вывод о возможности протекания реакции в данных условиях. Рассчитать константу равновесия для температур 298 К. Сделать вывод о состоянии равновесия. 4 NOг +6H2O(Ж)= 4NH3 + 5O2

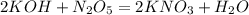
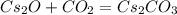
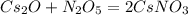
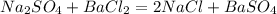
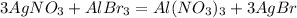
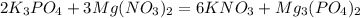
А какой класс? 7 или нет. ответь и я отвечу