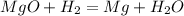ответ:6,978%
Объяснение:Уравнении реакции
4Р+5О2→2Р2О5 (1)
Р2О5+3Н2О→2Н3РО4(2)
Количество вещества фосфора
ν(Р)=9,3/31=0,3моль
Значить по реакции (1) образуется 0,15 моль Р2О5 и пореакции (2) образуется 0,3моль ортофосфорной кислоты.
Колличество вещества натрия: 6,9/23=0,3моль
Натрии реагирует с водой :
2Νа+2Н2О → 2ΝаОН+Н2(3)
а,гидроксид натрия с ортофосфорной кислотой
ΝаОН+Н3РО4 → ΝаН2РО4+Н2О(4)
По реакции (2) образуется 0,3 моль щелочи и 0,15моль водорода и по реакции (4) 0,3 моль ΝаН2РО4. Его масса 0,3*120=36г
масса раствора=9,3+500+6,9-0,3=515,9г
массовая доля дигроортофосфата натрия 36*100/515,9=6,978%
1)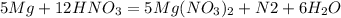
2)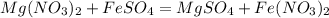
3)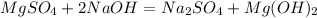
4)
5)