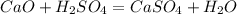
1) Нахом массу оксида кальция при 90%:
 г
г
2) Находим количество моль оксида кальция для того, чтобы через это узнать количество моль образовавшейся соли:
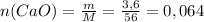 моль
моль
3) Смотри соотношение количества моль соли и оксида кальция. Зная соотношение, узнаём количество моль соли:
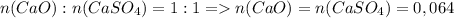 моль
моль
4) Теперь, когда мы знаем количество моль соли, то можем найти её массу:
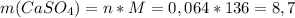 г
г
ответ: 8,7г
тка записать оба вещества в одну реакцию.
Получается примерно так:
«Смесь оксидов кальция и бария растворили в соляной кислоте…»
Уравнение реакции составляется так:
СаО + ВаО + 4HCl = СаCl2 + BaCl2 + 2H2O.
Это ошибка, ведь в этой смеси могут быть любые количества каждого оксида.
А в приведенном уравнении предполагается, что их равное количество.
Предположение, что их мольное соотношение соответствует коэффициентам в уравнениях реакций.
Например:
Zn + 2HCl = ZnCl2 + H2
2Al + 6HCl = 2AlCl3 + 3H2
Количество цинка принимается за х, а количество алюминия — за 2х (в соответствии с коэффициентом в уравнении реакции). Это тоже неверно. Эти количества могут быть любыми и они никак между собой не связаны.
Попытки найти «количество вещества смеси», поделив её массу на сумму молярных масс компонентов.
Это действие вообще никакого смысла не имеет. Каждая молярная масса может относиться только к отдельному веществу.
Часто в таких задачах используется р
Объяснение:
ОбъясРасцветали яблони и груши,
Поплыли туманы над рекой.
Выходила на берег Катюша,
На высокий берег на крутой.
Выходила на берег Катюша,
На высокий берег на крутой.
Выходила, песню заводила,
Про степного сизого орла.
Про того, которого любила,
Про того, чьи письма берегла.
Про того, которого любила,
Про того, чьи письма берегла.
Ой ты песня, песенка девичья,
Ты лети за ясным солнцем вслед
И бойцу на дальнем пограничье
От катюши передай привет
И бойцу на дальнем пограничье
От катюши передай привенение:
Дано:
m (тех CaO) = 4 г
W(СаО) = 90 %
Найти:
m(CaSO4)
Вычислим массу чистого CaO:
m(осн.комп) = m(тех.прод)\w(осн.комп) ∙ 100%
m(CaO) = 4 г ∙ 90% \100% = 3,6 г
Вычислим массу соли:
3,6 г х г
СaO + H2SO4 = CaSO4 + H2O
56 г 136 г
3,6 г --- х г
56 г --- 136 г
х = 3,6 г ∙ 136 г\56 г = 8,74 г
ответ: m(CaSO4) = 8,74 г