1)4 Li + O2 -›2Li₂O
2)4NH3 + 502 -›4NO+6H₂O
3) CaCO3 -›CaO+CO₂
4) Fe(OH)2 -›FeO+H₂O
5) Li2O + 2HNO3 -›2LiNO₃+H₂O
6) P2O3 + 3Ba(OH)2 -›Ba₃(PO₃)₂+3H₂O
7) BeO +2 LiOH -›Li₂BeO₂+H₂O
8) Al2O3 + K2O -›2KAlO₂
Кислоты (по количеству атомов водорода) разделяют на одноосновные (1 атом Н), двухосновные (2 атома) и трёхосновные.
По содержанию кислорода - на кислородсодержащие и безкислородные.
По силе - сильные, средней силы и слабые.
По устойчивости: устойчивые и неустойчивые.
По летучести (летучие (имеют запах) и нелетучие).
По растворимости в воде - растворимые и нерастворимые.
По содержанию атомов металла - металлосодержащие и неметаллосодердащие.
Реакции приложу ниже.
Получают кислоты следующим образом:
1). Неметаллы + водород.
2). Кислотные оксиды + вода.
3). Соль + кислота.
В быту применяются кислоты в качестве антисептиков, очищающих средств, при консервации (но это больше к органике).
* В реакции получения кислот с кислотных оксидов и воды у меня ошибка:
Должно быть Р2О5, а не Р2Н5.

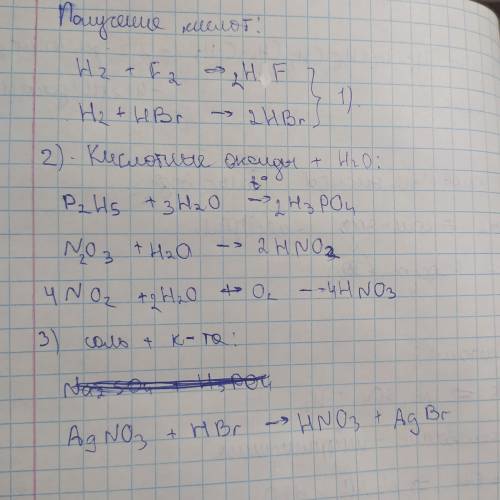
4Li + O₂ → 2Li2O
4NH₃ + 5O₂ → 4NO + 6H₂O
CaCO₃ → CaO + CO₂
Fe + 2H₂O → Fe(OH)₂ + H2
Li₂O + 2HNO₃ → 2LiNO₃ + H₂O
P₂O₃ + 3Ba(OH)₂ → Ba₃(PO3)₂ + 3H₂O
2LiOH + BeO → Li₂BeO₂ + H₂O
K₂O + Al₂O₃ → 2KAlO₂
Объяснение: