1) По определению массовая доля показывает массу растворенного вещества в 100 г раствора. Отсюда узнаем массу CuCl₂, которая будет содержаться в 500 г 2% раствора:
100 г раствора содержит 2 г CuCl₂
500 г раствора содержит х г CuCl₂
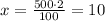 г CuCl₂
г CuCl₂
2) Теперь расчитаем массу раствора 8%, которую нужно будет взять для приготовления 2% раствора (расчитаем массу раствора, в котором будет содержаться 10 г CuCl₂):
100 г раствора содержит 8 г CuCl₂
х г раствора содержит 10 г CuCl₂
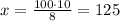 г раствора
г раствора
3) Раз нам дана масса конечного 2% раствора, расчитаем массу воды, которую необходимо добавить к нашему 8% раствору:
m(H₂O)=500-125=375 г
ответ: для приготовления 500 г 2% раствора потребуются 125 г 8% раствора и 375 г воды.
BaCO3+2HCl=BaCl2+H2O+CO2
Na2CO3+2HCl=2NaCl+H2O+CO2
BaCl2+Na2SO4=BaSO4(осадок)+2NaCl
в осадок в результате обработки избытком сульфата натрия выпадает сульфат бария (идет только реакция с хлоридом бария, реакция с хлоридом натрия не идет)...
количество вещества сульфата бария, выпавшего в осадок: m(BaSO4)/M(BaSO4)=(46.6г)/(233г/моль)=0,2 моль
карбоната бария было также 0,2 моль...
зная количество вещества и молярную массу карбоната бария (197 г/моль), находим массу карбоната бария: 0,2*197=39,4 г.
теперь находим долю карбоната бария в его смеси с карбонатом натрия:
m(BaCO3)*100%/(m(BaCO3)+m(Na2CO3))=39.4*100/50=78.8%
Масса CuCl2 в 500граммовом растворе равна (500г*2%)/100%=10г
Масса CuCl2 в начальном растворе будет такая же.
Масса начального раствора равна (10г*100%)/8%=125г
Соответственно, чтобы получить 500граммовый раствор, нужно добавить 500-125=375 грамм воды.