n CO2 = v/молярный объём = 1,12л/22,4л/моль = 0,05 моль
Уравнение реакции: 2KOH+CO2 = K2CO3+H2O
по уравнению р-ии n K2CO3 = n CO2 = 0,05 моль
m K2CO3 = n*M = 0,05 моль*138г/моль = 6,9г
w K2CO3 = m K2CO3/m раствора*100% = 6,9г/130г*100% = 0,0531*100% = 5,31%
ответ: 5,31%.
1) Берём 5-7 капель раствора (NH4)2SO4 и 1-2 капли концентрированного раствора NaOH, к примеру. )
Происходит реакция:
(NH4)2SO4 + 2NaOH(конц.) = Na2SO4 + 2NH3↑ + 2H2O (при нагревании)
Выделяется аммиак(газ). Он достигает влажной лакмусовой или фенолфталеиновой бумажки. Так как она влажная, то аммиак соединяется с водой, образуя гидроксид аммония. NH3 + HOH = NH4OH
Гидроксид аммония даёт щелочную среду, поэтому лакмусовая бумажка - синий цвет, фенолфталеин - фиолетовый(малиновый).
Получается, что качественная реакция на соли аммония у нас - это добавление концентрированной щёлочи и выделение аммиака, который окрашивает индикатор во влажной среде в соответствующий цвет(его реакция на щелочную среду).
2) Al(NO3)3 + 3NaOH = Al(OH)3(осадок) + 3NaNO3 - при первичном добавлении раствора щелочи.
Al(OH)3 + NaOH = Na[Al(OH)4] - при последующем добавлении щёлочи образуется комплексная соль тетрагидроксоалюминат натрия(Al(OH)3 проявляет кислотные свойства)
Сделайте вывод о распознавании солей аммония.Это наверное к первому пункту =) Мы уже вывод по поводу качественной реакции на соли аммония сделали.
3.36л
Объяснение:
Реакция взаимодействия натрия с кислородом описывается следующим уравнением:
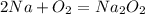
Молярная масса натрия равна 23 г/моль, значит количество вещества натрия равна 6.9/23 = 0.3 моль
По уравнению кислород требует в два раза меньше (там же коэффициент равен 1, а соотношение коэффициентов натрия к кислороду равно 2:1) количество вещества, т.е. 0.15 моль, а объем становится равным 22.4 * 0.15 = 3.36 л (как произведение молярного объема, который при нормальных условиях всегда равен 22.4 л/моль, на количество вещества кислорода, который равен 0.15 моль)
2КОН+СО2= К2СО3+Н20
ню(СО2)= 1,12:22,4= 0,05 моль= ню ( К2СО3)
m(K2CO3)чистого вещ-ва= 0,05*138= 6,9 г
w= 6,9:130*100%=5,3 %