A) CaF2 - фторид кальция - ионная связь - схема у молекулы линейная
Б) AsH3 - гидрид мышьяка - ковалентная полярная связь - схема молекулы представляет тэтраэдр

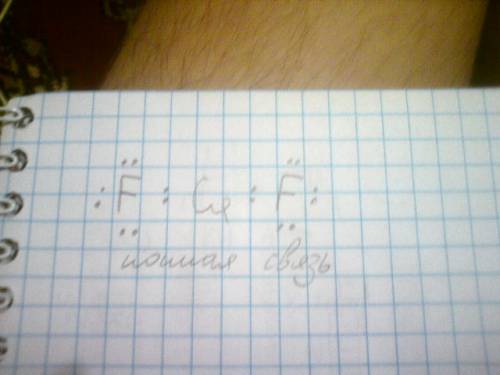
1. Физическое явление (изменение агрегатного состояния воды).
2. Химическое явление: протекает реакция взаимодействия гидрокарбоната натрия с уксусной кислотой с выделением углекислого газа и воды.
3. Химическое явление: взаимодействие гидроксида кальция с углекислым газом с образованием осадка карбоната кальция (помутнение) и воды.
4. Химическое явление: окисление железа кислородом воздуха с образованием оксида железа (III).
5. Химическое явление: медь взаимодействует с углекислым газом, кислородом и водяными парами с образованием гидроксокарбоната меди (II).
6. Физическое явление: пузырьки газа из растворенного состояния переходят в свободное, в атмосферный воздух.
Объяснение:
опыт 1. Получение раствора гидроксида кальция. Небольшой кусочек мела СаСОз захватить тигельными щипцами и прокаливать 3-5 мин, охладить, поместить в фарфоровую чашку или пробирку и, смочив несколькими каплями воды, наблюдать за изменениями. После этого прибавить 2-3 капли раствора фенолфталеина и сделать вывод о характере раствора. Написать уравнения реакций, происходящих при прокаливании СаСОз и растворении продукта прокаливания.
Опыт 2. Взаимодействие основного оксида с водой» К небольшому количеству оксида магния в пробирке прилить дистиллированной воды и взболтать. Прибавить к реакционной смеси 2-3 капли раствора фенолфталеина. Что наблюдается? Написать уравнения реакции.
Опыт 3. Получение нерастворимых в воде гидроксидов. В две пробирки налить по 1-2 мл раствора солей FeCl3 и CuSO4 и прибавить приблизительно равный объем раствора гидроксида натрия. Что наблюдается? Испытать в воде, кислоте и щелочи растворимость полученных осадков. Написать уравнения реакций.
2СН3COONa + H2SO4 = 2CH3COOH + Na2SO4 2NaCl + H2SO4(конц) = Na2SO4 + 2HCl↑
Объяснение:
А. Ca+F2=CaF2 - ионная
Б. 2As + 3H2 = 2AsH3 - ковалентная