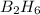Молярная масса соед-ия сос-т 28 г/моль (раз 1 л соед-ия имеет массу равную массе 1 л азота, след-но 22.4 л соед-ия имеет массу = массе 22.4 л азота (M N2 = 28 г/моль)); т.о. кол-во в-ва B сос-т (28*0.782)/11 = 2 моль, а кол-во в-ва H - соот-но (28*(1-0.782))/1 = 6 моль, что приводит к прос-й ф-ле B2H6 (M = 28 г/моль, след-но простейшая ф-ла явл-ся истинной ф-ой).
1. Определим массу 1 моль соединения бора:
1 моль азота, а это 22,4 л имеет вес 28 г, а значит и соединение бора имеет вес 28 г
2. Теперь определим количество атомов бора и водорода:
Вот и выходит формула: