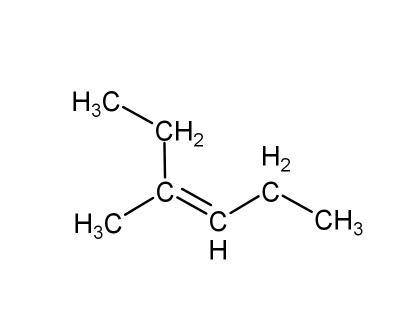
CH3C(CH2CH3)=CHCH3
Объяснение:
см. фото
H2CO3+Mg(OH)2=MgCO2+2H2O
для кислот эквивалент равен 1 поделенной на количество атомов водорода, отданных кислотой в ходе реакции. Значит здесь эквивалент Н2СО3 равен 1/2. Молярная масса эквивалента Мэ = М*Э (М - молярная масса вещества, Э - эквивалент этого вещества). Значит, Мэ = 62*1/2 = 31 г/моль
2H2CO3+CaCO3=Ca(HCO3)2+H2O
Одна молекула кислоты отдает один атом водорода в ходе реакции. Э = 1/1 = 1. Мэ = 62*1 = 61 г/моль.
H2CO3+2KOH=K2CO3+2H2O
Молекула уислоты в ходе реакции отдает оба атома водорода, значит Э = 1/2. Мэ = 62/2 = 31 г/моль.
C2H2+2Br2=CBr2-CBr2
| |
H. H
x/26=86,5/346
x=6,5
x/64=6,5/26
x=16
w=m(CaC2)*100%/m(тех)=16*100/20=80%