ответ:Метан має такі хімічні властивості. Він горить, утворюючи вуглекислий газ і воду.
CH4 + 2O2 → CO2 + 2H2O.
Горіння метану супроводжується виділенням великої кількості теплоти. У разі нестачі кисню метан окиснюється не повністю. І тоді замість карбон(IV) оксиду CO2 утворюється карбон(II) оксид CO, відомий як чадний газ.
2CH4 + 3O2 → 2CO + 4H2O.
При нагріванні метан може розкладатися на прості речовини вуглець і водень. Це реакція повного розкладу.
CH4 → C + 2H2
А при температурі понад 1500 °С метан розкладається з утворенням ацетилену C2H2 і водню. Це реакція неповного розкладу або дегідрування.
2CH4 → C2H2 + 3H2
За звичайних умов метан не окислюється розчином калій перманганату, лугами і кислотами; не знебарвлює бромну воду.
Метан не вступає в реакції приєднання, але вступає в реакції заміщення. Серед реакцій заміщення найбільше значення мають реакції галогенуваня (хлорування, бромування) та нітрування. Реакція хлорування відбувається при освітленні суміші метану і хлору розсіяним ультрафіолетовим промінням (або при нагріванні).
Объяснение:
Задача №1
- Уравнение:
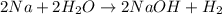
- вычислим количество вещества водорода:
n = V/Vm = 4,48л/22,4л/моль = 0,2 моль
- По уравнению реакции:
n(Na) = 2n(H2) = 0.2моль*2 = 0,4 моль
- Вычисляем массу натрия:
m(Na) = n*M = 0,4моль*23г/моль = 9,2 грамма
Отвеот: масса натрия равна 9,2 грамма
Задача №2
- Уравнение:
CuO + H2 = Cu + H2O
-По уравнению реакции, видим, что:
n(H2) = n(CuO) = 1,5 моль
- Масса 1,5 моль водорода:
m= n*M = 2г/моль*1,5моль = 3 грамма
- По уравнению реакции, видим, что:
n(Cu) = n(CuO) = 1.5 моль
- Рассчитывеам массу 1,5 моль меди:
m = n*M = 1,5 моль*64г/моль = 96 грамм
6CO₂ + 6H₂O ---> C₆H₁₂O₆ + 6O₂
2C₆H₁₂O₆ ---> C₁₂H₂₂O₁₁ + H₂O
nC₁₂H₂₂O₁₁ --> (-C₆H₁₀O₅-)n + nH₂O
(-C₆H₁₀O₅-)n + 6nO₂ --> 6nCO₂ + 5nH₂O