1) BaCl2+K2CO3=2KCl+BaCO3(осадок)
Ba(2+) + 2Cl(-) + 2K(+) + CO3(2-) = 2K(+) + 2Cl(-) + BaCO3
Ba(2+) + CO3(2-) = BaCO3
2) HCl+NaOH=NaCl+H2O
H(+) + Cl(-) + Na(+) + OH(-) = Na(+) + Cl(-) + H2O
H(+) + OH(-) = H2O
3) 2HCl+Cu=H2+CuCl(осадок)
2H(+) + 2Cl(-) + Cu(2+) = 2H(+) + CuCl
2Cl(-) + Cu(2+) = CuCl
4) NaOH+Ca=Ca(OH)2(осадок)+2Na
2Na(+) + 2OH(-) + Ca(2+) = Ca(OH)2 + 2Na(+)
2OH(-) + Ca(2+) = CaCO3
5) K2CO3+ Ca=CaCO3(осадок)+2K
2K(+) + CO3(2-) + Ca(2+) = CaCO3 + 2K(+)
CO3(2-) + Ca(2+) = CaCO3
6) K2O+2HCl=2KCl+H2O
K2O + 2H(+) + 2Cl(-) = 2K(+) + 2Cl(-) + H2O
K2O = 2K(+) + H2O
7) K2O++2NaOH=2KOH=Na2O
K2O + 2Na(+) + 2OH(-) = 2K(+) + 2OH(-) + NaO
K2O + 2Na(+) = 2K(+) + NaO
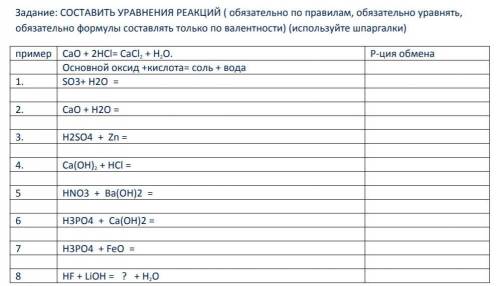
SO3+H2O=H2SO4 реакция присоединения
CaO+H2O=Ca(OH)2 реакция присоединения
H2SO4+Zn=ZnSO4+H2 реакция замещения
Ca(OH)2+2HCl=CaCl2+2H2O реакция обмена
2HNO3+Ba(OH)2=Ba(NO3)2+2H2O реакция обмена
2H3PO4+3Ca(OH)2=Ca3(PO4)2+6H2O реакция обмена
2H3PO4+3FeO=Fe3(PO4)2+3H2O реакция обмена
HF+LiOH=LiF+H2O реакция обмена