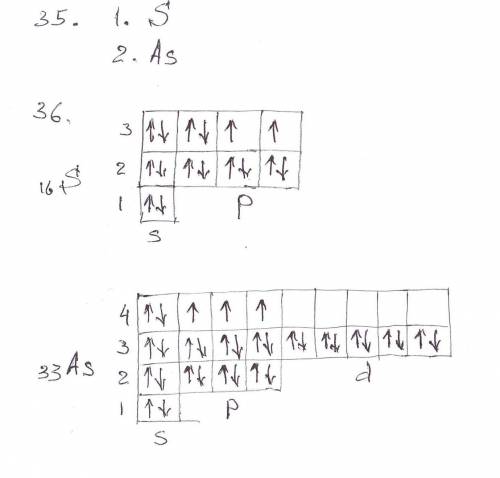
36. Дописать название подуровня и его номер. Записать химический знак элемента и перед ним поставить его порядковый номер. (См. в файл)
37. Номеру данного периода.
38. Номеру группы.
39. Количеством валентных электронов, т.е. электронов на внешнем слое.
40. Изменением строения их электронных оболочек. В каждом периоде происходит заполнение электронами внешнего энергетического уровня до восьми. Следовательно, электронные конфигурации наружных энергетических уровней периодически повторяются.
41. s-элементы - это элементы главной подгруппы I и II групп. По факту это элементы у которых заполняется s-уровень. В каждом периоде по 2 s-элемента.
42. р-элементы - это элементы III-VIII групп, главных подгрупп. Это элементы у которых заполняется р-уровень. Всего 6 р-элементов в каждом периоде (кроме первого, их там нет; и седьмого - хотя там тоже их 6 штук).
43. d-элементы - это элементы I-VIII групп, побочных подгрупп. Это элементы у которых заполняется d-уровень. В каждом большом периоде по 10 d-элементов.
Объяснение:
Объяснение:
Чтобы ответить на вопрос «как определить валентные электроны» нужно для начала определиться с самим понятием валентных электронов.
Атом химического элемента состоит из положительно заряженного ядра, внутри которого находятся протоны и нейтроны, а вокруг него по орбитам движутся электроны. Орбитали, которые расположены дальше всего от ядра носят название внешних (внешний энергетический уровень), а электроны, расположенные на них – внешних или валентных. Именно эти электроны отвечают за образование химической связи с другими атомами.
Общее количество валентных электронов можно определить при Периодической таблицы Д.И. Менделеева. Номер группы, в которой находится интересующий вас элемент, вне зависимости от подгруппы (главная или побочная), равен числу электронов на внешнем энергетическом уровне. Например, Na расположен в I группе, значит у него 1 валентный электрон, Al в III группе – 3 валентных электрона и т.д.
Чтобы определить, электроны, расположенные на каких подуровнях, являются валентными для элементов разных семейств, нужно записать электронную конфигурацию атома в основном состоянии. Рассмотрим на примере Li (s-элемент), S (p-элемент), Cr (d-элемент) и La (f-элемент).




Для s-элементов валентными считаются электроны, расположенные s-орбитали, p-элементов – сумма электронов, расположенных на s- и p-орбиталях внешнего уровня; d-элементов — сумма электронов, расположенных на s- и d-орбиталях внешнего уровня; f- элементов — сумма электронов, расположенных на s- и d-орбиталях внешнего уровня.