1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
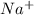

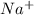
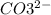

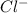


Ca, Ba, Mg
2.SO3
3.CH4 : C ( IV ) ; H( I );
SO3 : S ( VI ) ; O ( II );
NH3 : N ( III ) ; H ( I );
H2S : H ( I ) ; S ( II );
4.а ) Al2S3;
б) P2O5
в) CCl4
г) MgO
5.Mr ( H2CO3 ) = 12 + 1 x 2 + 16 x 3 = 62
Объяснение:Валентность - свойство атома соединяться с некоторым количеством других атомов, или образовывать некоторое количество химических связей
Валентные возможности атома зависят от: 1) Количества электронов на внешнем уровне, например:У Магния на внешнем уровне два электрона, по этому валентность магния - II
2) Количества неспаренных электронов:В Кислороде два неспаренных электрона, то есть валентность - II
3) Наличия свободных орбиталей:В Углероде есть два не спаренных электрона, а так же свободная орбитально, на которую один из электронов на 2s орбитали может "перейти" на 2p орбиталь, по этому у него в нормальном состоянии валентность - II, а в возбужденном - IV
Атом углерода проявляет четвертую валентность, так как может иметь 4 неспаренных электрона
Поэтому валентность бывает постоянная и переменная
Валентность могут иметь и группы атомов:валентность - I :OH - гидроксогруппа;
NH4 - группа амония;
NH2 - аминогруппа;
NO2 - нитрогруппа;
NO3 - кислотный остаток нитрат.
валентность - II :кислотные остатки:
SO4 - сульфат;
SO3 - сульфит
CO3 - карбонат
SiO3 - силикат
валентность - III :PO4 - кислотный остаток фосфат ( или ортофосфат )