
(разб.) + KOH = H2O + KNO3
Полнаяформа:
K+ + OH− + H+ + NO3− = K+ + NO3− + H2O
Краткаяформа:
OH− + H+ = H2O
HNO3 + KOH = H2O + KNO3
Полнаяформа:
K+ + OH− + H+ + NO3− = K+ + NO3− + H2O
Краткаяформа:
OH− + H+ = H2O
HNO3(разб.) + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
HNO3 + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
HNO3(разб.) + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
HNO3 + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
HNO3(разб.) + KOH = H2O + KNO
Полнаяформа:
K+ + OH− + H+ + NO3− = K+ + NO3− + H2O
Краткаяформа:
OH− + H+ = H2O
Химаша | решаю реакции по химии, [28.12.2020, 22:40]
HNO3 + KOH = H2O
Полнаяформа:
K+ + OH− + H+ + NO3− = K+ + NO3− + H2O
Краткаяформа:
OH− + H+ = H20
HNO3(разб.) + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
HNO3 + KOH = H2O + KNO3
Полнаяформа:K+ + OH- + H+ + NO3- = K+ + NO3- + H2O
Краткаяформа:OH- + H+ = H2O
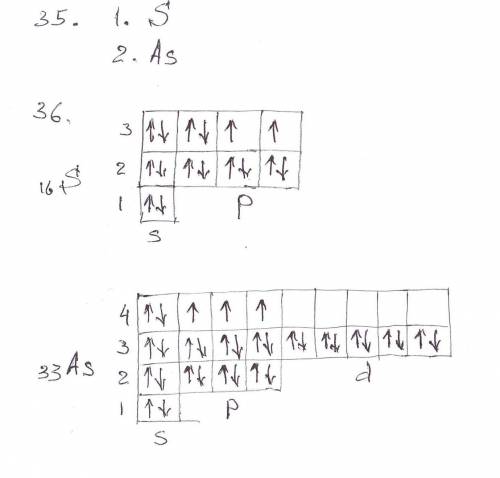
36. Дописать название подуровня и его номер. Записать химический знак элемента и перед ним поставить его порядковый номер. (См. в файл)
37. Номеру данного периода.
38. Номеру группы.
39. Количеством валентных электронов, т.е. электронов на внешнем слое.
40. Изменением строения их электронных оболочек. В каждом периоде происходит заполнение электронами внешнего энергетического уровня до восьми. Следовательно, электронные конфигурации наружных энергетических уровней периодически повторяются.
41. s-элементы - это элементы главной подгруппы I и II групп. По факту это элементы у которых заполняется s-уровень. В каждом периоде по 2 s-элемента.
42. р-элементы - это элементы III-VIII групп, главных подгрупп. Это элементы у которых заполняется р-уровень. Всего 6 р-элементов в каждом периоде (кроме первого, их там нет; и седьмого - хотя там тоже их 6 штук).
43. d-элементы - это элементы I-VIII групп, побочных подгрупп. Это элементы у которых заполняется d-уровень. В каждом большом периоде по 10 d-элементов.
Объяснение:
1.Нітроген N знаходиться у 2 періоді, має валентність V,
Протонне число 7
Кількість електронів 7
Кількість протонів 7
Кількість нейтронів 14-7=7
Фосфор Р знаходиться у 3 періоді, має валентність VПротонне число 15
Кількість електронів 15
Кількість протонів 15
Кількість нейтронів 31-15= 16
2. на фото + металічні властивості, бо це метал
3. У хлору. Тому що на таблиці радіусів атомів хлор знаходиться далі від атомів металічних елементів і має менший радіус від силіцію, а силіцій ближче та має більший радіус(2фото)
Вроде бы правильно :)