1) Визначте роботу розширення 10 л газу при ізобарному нагріванні від 30 °С до 150 °С. Тиск газу 100 кПа. 2) Яку роботу може виконати кисень масою 8 г при ізобарному підвищенні температури на 100 К?
4)А - я бы сказал не предыдущим, а последующим гомологом
5)А
6)В
7)А
8)Б
9)В
10)В
11) C₂H₅OH --H₂SO₄--> C₂H₄ + H₂O
C₂H₄ + HCl --> C₂H₅Cl
2C₂H₅Cl + 2Na --> C₄H₁₀ + 2NaCl
12) Формула C₅H₁₀
Межклассовая изомерия
CH₂=CH-CH₂-CH₂-CH₃ пентен-1
CH₃-CH=CH₂-CH₂-CH₃ пентен-2
Измерия углеродной цепи:
CH₂-CH-CH₃ метилциклобутан
| |
CH₂-CH₂
13) арены используются для производства ядов для насекомых и грызунов, их гомологи для производства красок смол , в качестве растворителей, в орг. синтезе
14)
Молярная масса углеводорода: M = D(H₂)*M(H₂) = 14*2=28 г/моль
На 100 г соединения приходится 85,7 г С и 14,3 г Н (в решении опечатка где-то - должно быть не более 100% суммарно).
Соотношение количеств элементов:
n(C) : n(H) = = 7,14 : 14,3 = 1:2
Формула CH₂
А так как молярная масса 28 г/моль, то C₂H₄, т.е. этен
Однако ни в коем случае при разбавлении нельзя добавлять воду в кислоту. Существует строгое правило: лить кислоту в воду! Нарушение этого правило может привести к трагедии. Дело в том, что при приготовлении растворов часто происходит их разогрев. При приготовлении растворов серной кислоты происходит сильный разогрев. Представьте себе, что будет, если нарушить правило, и добавить воду в кислоту. Вода, попав в массу концентрированной кислоты, моментально разогреется до кипения - произойдет мощный и опасный выброс кислоты.
1)Б
2)В
3)А - не это не изомер, а это же вещество
4)А - я бы сказал не предыдущим, а последующим гомологом
5)А
6)В
7)А
8)Б
9)В
10)В
11) C₂H₅OH --H₂SO₄--> C₂H₄ + H₂O
C₂H₄ + HCl --> C₂H₅Cl
2C₂H₅Cl + 2Na --> C₄H₁₀ + 2NaCl
12) Формула C₅H₁₀
Межклассовая изомерия
CH₂=CH-CH₂-CH₂-CH₃ пентен-1
CH₃-CH=CH₂-CH₂-CH₃ пентен-2
Измерия углеродной цепи:
CH₂-CH-CH₃ метилциклобутан
| |
CH₂-CH₂
13) арены используются для производства ядов для насекомых и грызунов, их гомологи для производства красок смол , в качестве растворителей, в орг. синтезе
14)
Молярная масса углеводорода: M = D(H₂)*M(H₂) = 14*2=28 г/моль
На 100 г соединения приходится 85,7 г С и 14,3 г Н (в решении опечатка где-то - должно быть не более 100% суммарно).
Соотношение количеств элементов:
n(C) : n(H) =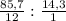 = 7,14 : 14,3 = 1:2
= 7,14 : 14,3 = 1:2
Формула CH₂
А так как молярная масса 28 г/моль, то C₂H₄, т.е. этен