Задача № 3. Получите сульфат железа (II) не менее чем тремя
Опыт 1.
В пробирку опустите 2-3 кусочка железа. Прилейте 1-2мл раствора сульфата меди(II). Что наблюдаете? Запишите уравнение реакции. Составьте схему электронного баланса.
Опыт 2.
В пробирку опустите 2-3 кусочка железа. Прилейте 1-2мл раствора соляной кислоты. Что наблюдаете? Запишите уравнение реакции. Составьте схему электронного баланса.
Опыт 3.
В пробирку налейте 1-2мл раствора хлорида железа(II) и добавьте к нему 3-4 капли раствора гидроксида натрия. К полученному осадку прилейте раствор серной кислоты. Что наблюдаете? Запишите уравнение реакции в молекулярном и ионном виде.
№1
m(соли)=127 г
m(H2O)=2000 г
ω=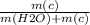 *100%=~5.97%
*100%=~5.97%
№2
m(р-ра)=150 г
ω=15%
ω=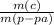 *100%
*100%
m(c)=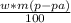 =22,5 г
=22,5 г
(100 процентов если что. так что это считай делить на 1)
№3
ω=27%
m(с)=87 г
ω=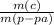 *100%
*100%
m(p-pa)=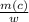 *100%
*100%
m(p-pa)=~322,2 г.
1)5.97%
2)22.5 г
3)322.2 г