Дано:
m(Ca)= 20 (г)
Найти: m(CaO)=?(г)
20(г). Х(г)
2Ca+O2=> 2CaO
Над Ca пишем 20 (г)
Под ним пишем
n(Ca)= 2 (моль) (в реакции перед Са стоит 2)
M(Ca)= 40 (г/моль) (смотрим по таблице Менделеева, атомная масса кальция = 40.
m(Ca)= n(Ca)*M(Ca)=80 (г)
Над CaO пишем Х(г)
Под ним пишем
n(CaO)= 2 (моль) (в реакции перед СаО стоит 2)
M(CaO)= 56 (г/моль) (по таблице Менделеева смотрим атомную массу, Ar(Ca)= 40; Ar(O)=16 M(CaO)= Ar(Ca)+Ar(O)=40+16=56
m(CaO) = n(CaO)*M(CaO)=112 (г)
Составим и решим пропорцию основываясь на полученные данные.
20(г)/80(г):Х(г)/112(г)
Х(г)= 20(г)*112(г)/80(г)= 28 (г)
ответ: m(CaO)= 28 (г)
1. Тип химической связи в соединении Н2О: в) ковалентная полярная
2. Наиболее электроотрицательный химический элемент: б) Cl
3. Заряд иона кальция: а) 2+
4. Завершенный внешний электронный слой имеет атом химического элемента: а) Не
5. Число общих электронных пар между атомами в молекуле О2 равно:
б) 2
О=О
6. Ковалентная неполярная связь образуется между:
а) атомами одного неметалла
7. Сущность ионной связи состоит:
а) в электростатическом притяжении между разноименными зарядами
(ионами)
8. Электроотрицательность химических элементов в периодах с увеличением порядкового номера элемента:
а) увеличивается
9. К правильным утверждениям относятся:
а) соединяясь между собой, атомы стремятся к достижению устойчивого состояния
г) между калием и хлором образуется ионная связь
10. В периоде слева направо радиус атома и металлические свойства
соответственно: г) уменьшается и уменьшаются
11. Внешний уровень считается завершенным (кроме водорода и гелия), если на нем:
тогда г) 8 электронов
12. Образование молекулы водорода из атомов, можно изобразить:
г) H • + • H → H •• H
13. В какой молекуле тройная связь? а) N2
14. Выберите элемент с переменной валентностью:
а) Cl
15. При образовании ковалентной полярной связи электронная пара:
г) смещена к более электроотрицательному элементу
16. В каком соединении валентность железа равна III?
в) Fe2O3
17. Ковалентная полярная связь образуется между:
в) различными атомами неметаллов
18. В ряду элементов: Al Si P S: ?????
а) увеличивается число электронных слоев в атомах;
б) усиливаются неметаллические свойства;
в) уменьшается число внешних электронов в атомах;
г) возрастают радиусы атомов.
19. Напишите электронную и электронно-графическую формулы для атома Са.
+20 ) ) ) ) 1s² 2s² 2p⁶ 3s² 3p⁶ 4s₂
2882
Укажите валентность элемента = II.
20. Запишите электронные и графические схемы образования молекулы HCl..
в фото
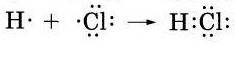
2NaCl + 2Н 2 О электролиз → H 2 ↑ +2NaOH + Cl 2 ↑ . Масса хлорида натрия равна m = 500⋅0,2 = 100 г. Согласно формуле (6.4.1) имеем: V (H2) = QVэ (H2) / 96 500, отсюда Q = V(H2)⋅96500 / Vэ(H2) = 1,12⋅96 500 / 11,2 = 9650 Кл. m(NaCl) = 9650⋅58,5 / 96 500 = 5,85 г; m(NaOH) = 40⋅9650 / 96 500 = 4,0 г. Оставшаяся масса хлорида натрия равна 100,0 – 5,85 = 94,15 г; m(H2O) = 9⋅9650 / 96 500 = 0,9 г. П р и м е р 131 При электролизе водного раствора нитрата никеля(II) (ω = 50 %) массой 91,50 г на катоде выделился никель массой 14,75 г. Определите содержание азотной кислоты в растворе (ω, %) после электролиза и объем газа, выделив- шегося на аноде. Решение Уравнение электролиза водного раствора нитрата никеля(II) Ni(NO 3 ) 2 + 2H 2 O электролиз → Ni + 2HNO 3 + O 2 ↑ + H 2 ↑ M(Ni) = 59 г/моль; М(HNO3) = 63 г/моль. Количество никеля, выделенного на катоде равно 14,75/59 = 0,25 моль. Следовательно, по реакции образуется 0,5 моль HNO3 или 0,5⋅63 = 31,5 г. Количество кислорода составит 0,25 моль 0,25⋅22,4 = 5,6 дм3 или 8,0 г. Такой же объем водорода выделяется на катоде, т.е. 5,6 дм3 или 0,5 г. Масса раствора составит 91,50 – 14,75 – 8,50 = 68,25 г. Откуда ω(HNO3) = 31,50⋅100/68,25 = 46,5 %.