2Fe₂S₃⁻² + 9O₂⁰ = 2Fe₂O₃⁻² + 6S⁺⁴O₂
S⁻² - 6e⁻ = S⁺⁴ | 1 - восстановитель, процесс окисления
O₂⁰ + 2e⁻ = 2O⁻² | 3 - окислитель, процесс восстановления
2) O₂(г)+2NO(г)=2NO₂(г)+Q
Реакция соединения, экзотермическая, окислительно-восстановительная
3) 2NO(г)+O₂(г)=2NO₂(г)+Q
По УХР видим, что реакция экзотермическая, идет с уменьшением объема, согласно принципа Ле Шателье повышение давления в данном случае приведет к смещению равновесия в сторону образования продукта реакции (вправо), снижение температуры также приведет к смещению равновесия в сторону образования продукта реакции (вправо), повышение концентрации одного из реагентов или снижение концентрации продукта реакции также приведет к смещению равновесия в сторону образования продукта реакции (вправо).
4. 4NH3+5O2=4NO+6H2O
До изменения концентрации скорость реакции выражалась уравнением:
v₁= k[NH₃]⁴[O₂]⁵
После уменьшения концентрации NH₃ в 2 раза
v₂ = k(¹/₂[NH₃])⁴[O₂]⁵ = 0.0625k[NH₃]⁴[O₂]⁵
v₁/v₂ = ¹/0.0625 = 16
Скорость реакции уменьшится в 16 раз.
5.
(60-30) = 30 30/10=3
2³ = 8
Скорость реакции уменьшится в 8 раз
6.
М(С₂Н₄) = 28 г/моль
n(С₂Н₄) = 112 г/28 г/моль = 4 моль
C₂H₄+3O₂=2CO₂+2H₂O
Q = Q'/n = 5292 кДж/4 моль = 1323 кДж/моль
ответ: C₂H₄+3O₂=2CO₂+2H₂O + 1323 кДж
х г 12 л
106 г 22,4 л
1. Знайдемо чисту масу кальцинованої соди:
при взаємодіїї 106 г соди віділяється 22,4 л вуглекислого газу, а
при -- // -- х г_________________12 л, звідки
х=106*12/22,4=57 г
2. Тепер,віднявши від загальної маси зразка отриману чисту масу соди,отримаємо масу домішків:
m(домішків)=m(зразка) - m(Na2CO3)=68 - 57 =11 г
3. Віднесемо масу домішків до загальної маси зразка і отримаємо масову частку домішків:
w(домішків)=m(домішків)/m(зразка)=11/68=0,16 або 16%
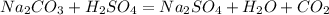
20 л. Х л
2C2H2. +. O2. =. 4CO2. +. 2H2O
n=2 моль. n=4 моль
Vm=22,4 л/моль Vm=22,4 л/моль
V=44,8 л. V=89,6 л
20 л. С2Н2. -. Х л. СО2
44,8 л С2Н2 -. 89,6 л СО2
V(CO2)=20*89,6/44,8=40 л