1) Гидрирование (с образованием первичных спиртов):
H₃C-COH+H₂→H₃C-CH₂-OH
2) Присоединение гидросульфита натрия (только для алициклических):
H₃C-COH+NaHSO₃→H₃C-C-SO₃Na
|
OH
3) Присоединение синильной кислоты (образование гидроксинитрилов, или циангидринов): H₃C-COH+HCN→H₃C-CH-CN
|
OH
4) Присоединение спиртов (образование ацеталей):
R-COH+H₃-CH₂-OH⇄R-CH-O-CH₂-CH₃
| полуацеталь
OH
R-CH-O-CH₂-CH₃ R-CH-O-CH₂-CH₃
| +H₃C-CH₂-OH⇄ | ацеталь
OH O-CH₂-CH₃
5) Гидратация: CH₂=O+H₂O→H₂C(OH)₂ гидрат формальдегида
6) Присоединение реактива Гриньяра:
R-COH+H₃C-CH₂-MgI→R-CH-CH₂-CH₃
|
O-MgI
R-CH-CH₂-CH₃ R-CH-CH₂-CH₃
| +H₂O→ | +Mg(OH)I
O-MgI OH
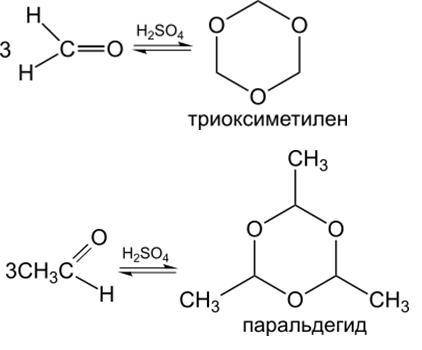
7) Полимеризация (циклическая и линейная)
7.1) линейная: под действием света происходит линейная полимеризация 40%-ного водного раствора формальдегида с образованием параформа (картинка внизу).
7.2) циклическая: альдегиды самопроизвольно или под действием кислот могут вступать в реакции тримеризации и тетрамеризации, при этом образуются шести- и восьмичленные циклы с чередующимися атомами углерода и кислорода в молекуле (картинка внизу).
8) Поликонденсация: реакции поликонденсации – это процесс образования полимеров из низкомолекулярных веществ, сопровождающийся отщеплением побочных низкомолекулярных веществ – воды, спирта, галогеноводородов и т.д. Альдегиды вступают в реакцию поликонденсации с фенолом (анилином и т.д.) с образованием соответствующих полимерных смол. Реакции протекают ступенчато: сначала образуется димер, затем тример и т.д. (картинка внизу).
9) Конденсация (картинка внизу).
10) Горение: CnH2nO+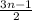 O₂→nCO₂↑+nH₂O
O₂→nCO₂↑+nH₂O
11) Реакции окисления. Альдегиды легко окисляются до кислот даже слабыми окислителями, такими как аммиачный раствор оксида серебра (Ag₂O/NH₃, или [Ag(NH₃)₂]OH), а также свежеосажденным гидроксидом меди (II):
11.1) реакция "серебряного зеркала": R-COH+2[Ag(NH₃)₂]OH→R-COONH₄ (или RCOOH) + 2Ag↓+3NH₃↑ (или 4NH₃↑)+H₂O
Исключение для формальдегида: HCOH+4[Ag(NH₃)₂]OH→(NH₄)₂CO₃+4Ag↓+6NH₃↑+2H₂O
11.2) R-COH+2Cu(OH)₂→R-COOH+Cu₂O↓+2H₂O
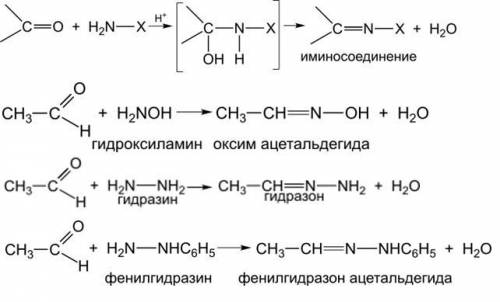
12) Реакции замещения с соединениями, содержащими аминогруппу (картинка внизу).
13) Взаимодействие с пентахлоридом фосфора:
R-COH+PCl₅→R-CH-Cl+POCl₃
|
Cl
14) Замещение атома водорода в радикале в α-положении к карбонильной группе (например, галогенирование). Сильно поляризованная карбонильная группа в молекулах альдегидов и кетонов вызывает понижение электронной плотности (δ+) на атомах углерода в α-положении, вследствие чего атомы водорода приобретают повышенную реакционную и могут отщепляться в виде протона:
H₃C-CH₂-CH₂-COH+Br₂→H₃C-CH₂-CH-COH+HBr
|
Br



Объяснение:
25. Лакмус имеет фиолетовую окраску.
Если будем приливать его к щедлочи гидроксиду натрия, то он начнет приобретать синюю окраску. Если прильем нитратную кислоту. Произойдет реакция нейтрализации и Лакмус начнет приобретать фиолетовую окраску.
NaOH+HNO₃=NaNO₃+H₂O
26. 2AICI₃+3Ba(OH)₂=2AI(OH)₃↓+3BaCI₂
2AI³⁺+6CI⁻+3Ba²⁺+6OH⁻=2AI(OH)₃↓+3Ba²⁺+6CI⁻
2AI³⁺+6OH⁻=2AI(OH)₃↓
27. Zn⁰+I₂⁰→Zn⁺²I₂⁻
Zn⁰-2e⁻→Zn⁺² 2 1
2I⁰+2xe⁻→2I⁻ 2 1
Zn⁰восстановитель, процесс окисления
I⁰окислитель, процесс восстановления
Zn+I₂→ZnI₂
28. Ca+2H₂O=Ca(OH)₂+H₂↑
29. H₂(г)+I₂(тв.)⇄HI(г.) ΔH=-18,8кДж.
Получение иодоводорода реакция эндотермическая, значит, чтобы сдвинуть реакцию вправо нужно повысить температуру.
30. Дано:
m(CuSO₄·5H₂O)=35г.
V(H₂O)=450мл. или
m(H₂O)=450г. так, как плотность воды ρ(H₂O)=1г./см
ω(CuSO₄)-?
1.M(CuSO₄)=160г./моль
M(CuSO₄·5H₂O)=250г./моль
3.m(р-ра) = m(СuSO₄ ·5H₂O)+m(H₂O) =35г.+450г. = 458г
4.m(СuSO₄)=m(СuSO₄ ·5H₂O)×[M(CuSO₄)÷M(CuSO₄·5H₂O)]=
=35г.× (160г./моль÷250г./моль) = 22,4г СuSO₄
5. ω(СuSO₄) =m(СuSO₄)÷m(р-ра) = 22,4÷485 = 0,04 или ω%(СuSO₄)=4%
6. ответ: массовая доля сульфата меди 4%
11
Объяснение:
см здесь