Закончите молекулярные уравнения возможных реакций, протекающих в растворах, и запишите соответствующие им ионные уравнения: а) HCI + Na2SO4 =>
б) H3PO4 + CaCI2 =>
в) FeCI3 + AgNO3 =>
г) KNO3 + NaCI =>
д) NaOH + FeS =>
е) KOH + AI2(SO4)3 =>
ж) Ca + CuCI2 =>
з) Cu + AgNO3 =>
и) Mg + ZnS =>
к) Cu + Fe(NO3)2 =>
![Ka= \frac{[H^{+}][CH_{3}COOH^{-}] }{[CH_{3}COOH]}](/tpl/images/0410/1569/d4237.png)
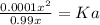 , где Ка - некая константа кислотности. Сократим х снизу и сверху и получим
, где Ка - некая константа кислотности. Сократим х снизу и сверху и получим
ω(CH₃COOH)=38%=0.38
p=1.05г/см³
m[р-ра (СH₃СO)₂O]=100г
ω[(CH₃CO)₂O]=35%=0.35
ω(CH₃COOH)=85%=0.85 - конечное
Найти:
V(р-ра СH₃COOH c ω=38%)-?
Решение:
(CH₃CO)₂O + H₂O = 2CH₃COOH
m[(CH₃CO)₂O]=100*0.35=35г
M[(CH₃CO)₂O]=102г/моль
M(CH₃COOH)=60г/моль
m₁(CH₃COOH)=(35*2*60)/102=41.18г - образовалось из уксусного ангидрида
m₂(CH₃COOH)=100-35=65г - было в растворе с уксусным ангидридом
Пусть масса (р-ра СH₃COOH c ω=38%) равна "х"(раствор который добавили).Тогда получаем:
0.85x+85=0.38x+106.18
0.47x=21.18
x=45г
m(р-ра СH₃COOH c ω=38%)=45г
V(р-ра СH₃COOH c ω=38%)=45/1.05=43см³
ответ: 43cм³.