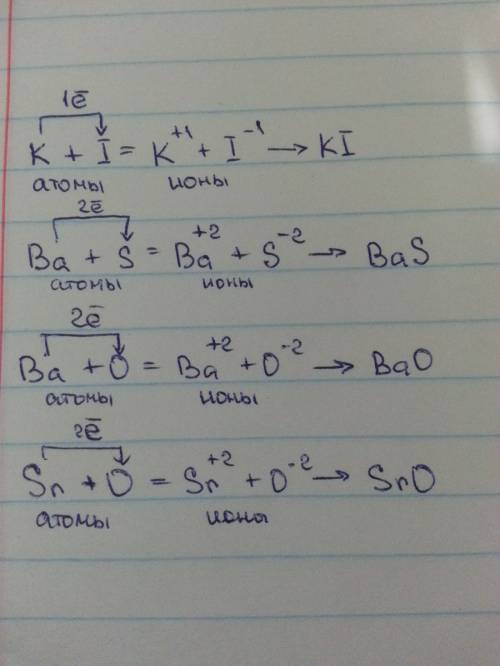
Соли взаимодействуют с кислотами и основаниями, если в результате реакции получается продукт, который выходит из сферы реакции (осадок, газ, мало диссоциирующие вещества, например, вода):
BaCl2(тверд.) + H2SO4(конц.) = BaSO4↓ + 2HCl↑
NaHCO3 + HCl(разб.) = NaCl + CO2↑ + H2O
Na2SiO3 + 2HCl(разб.) = SiO2↓ + 2NaCl + H2O
Соли взаимодействуют с металлами, если свободный металл находится левее металла в составе соли в электрохимическом ряде активности металлов:
Cu+HgCl2=CuCl2+Hg
Соли взаимодействуют между собой, если продукт реакции выходит из сферы реакции; в том числе эти реакции могут проходить с изменением степеней окисления атомов реагентов:
CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
NaCl(разб.) + AgNO3 = NaNO3 +AgCl↓
3Na2SO3 + 4H2SO4(разб.) + K2Cr2O7 = 3Na2SO4 + Cr2(SO4)3 + 4H2O + K2SO4
Некоторые соли разлагаются при нагревании:
CuCO3=CuO+CO2↑
NH4NO3 = N2O↑ + 2H2O
NH4NO2 = N2↑ + 2H2O
Объяснение:
9*10 в 23 13,44 л,х л у г
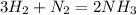
18*10 в 23 22,4 л 34 г
1. Сначала определим,какое из исходных веществ прореагирует полностью(без остатка),приняв одно из них за Х,например,объем азота:
для полного взаимодействия 18*10 в 23 водорода необходимо 22,4 л азота, а
для --//--//-- 9*10 в 23___________________х л, откуда
х=9*10 в 23*22,4/18*10 в 23=11,2 л
2. Как видим,что прореагирует водород полностью,так как азота вместо 11,2 л дано 13,44 л.Вот по количеству молекул водорода и найдем массу аммиака:
при взаимодействии 18*10 в 23 водорода образуется 34 г аммиака, а
при --//--//-- 9*10 в 23__________________у г, откуда
у=9*10 в 23*34/18*10 в 23=17 г