Разработка синтетических каучуков впервые началась в России в 1900 году учениками Бутлерова — Кондаковым, Фаворским, Лебедевым, Бызовым[2]. В 1900 году И. Л. Кондаков впервые получил синтетическим путём изопрен, изучением полимеризации которого занялся А. Е. Фаворский. В 1903—1910 годах параллельно группами учёных под руководством С. В. Лебедева и Б. В. Бызова велись работы по получению синтетического каучука на основе 1,3-бутадиена методом гидролиза нефтяного сырья[3]. Одновременно и независимо подобные работы велись в Англии. Впервые технология производства бутадиенового синтетического каучука разработана в лаборатории завода «Треугольник» Б. В. Бызовым, получившим за это изобретение в 1911 году премию имени Бутлерова[4]. Однако патент на это изобретение был оформлен только в 1913 году. Во время Первой мировой войны на заводе «Треугольник» был освоен выпуск противогазов из синтетического каучука Бызова[5].
Первый патент на процесс получения бутадиенового синтетического каучука с использованием натрия в качестве катализатора полимеризации был выдан в Англии в 1910 году. Первое маломасштабное производство синтетического каучука по технологии, сходной с описанной, в английском патенте имело место в Германии во время Первой мировой войны. Производство бутадиена в России началось в 1915 году по технологии, разработанной И. И. Остромысленским, позднее эмигрировавшим в США. В СССР работы по получению синтетического каучука были продолжены Бызовым и Лебедевым, в 1928 году разработавшим советскую промышленную технологию получения бутадиена. Коммерческое производство синтетического каучука началось в 1919 году в США (Thiokol), и к 1940 году в мире производилось более 10 его марок. Основными производителями были США, Германия и СССР[6]. В СССР производство синтетического каучука было начато на заводе СК-1 в 1932 году по методу С. В. Лебедева (получение из этилового спирта бутадиена с последующей анионной полимеризацией жидкого бутадиена в присутствии натрия)[7]. Прочность на разрыв советского синтетического каучука составляла около 2000 psi (для натурального каучука этот показатель составляет 4500 psi, для Неопрена, производство которого было начато компанией Du Pont (США) в 1931 году — 4000 psi). В 1941 году в рамках поставок по программе ленд-лиза СССР получил более совершенную технологию получения синтетического каучука[6].
В Германии бутадиен-натриевый каучук нашёл довольно широкое применение под названием «Буна»[de].
Синтез каучуков стал значительно дешевле с изобретением катализаторов Циглера — Натта.
Изопреновые каучуки — синтетические каучуки, получаемые полимеризацией изопрена в присутствии катализаторов — металлического лития, перекисных соединений. В отличие от других синтетических каучуков изопреновые каучуки, подобно натуральному каучуку, обладают высокой клейкостью и незначительно уступают ему в эластичности.
В настоящее время большая часть производимых каучуков является бутадиен-стирольными или бутадиен-стирол-акрилонитрильными сополимерами.
Каучуки с гетероатомами в качестве заместителей или имеющими их в своём составе часто характеризуются высокой стойкостью к действию растворителей, топлив и масел, устойчивостью к действию солнечного света, но обладают худшими механическими свойствами. Наиболее массовыми в производстве и применении каучуками с гетерозаместителями являются хлоропреновые каучуки (неопрен) — полимеры 2-хлорбутадиена.
В ограниченном масштабе производятся и используются тиоколы — полисульфидные каучуки, получаемые поликонденсацией дигалогеналканов (1,2-дихлорэтана, 1,2-дихлорпропана) и полисульфидов щелочных металлов.
Основные типы синтетических каучуков:
Изопреновый
Бутадиеновый
Бутадиен-метилстирольный
Бутилкаучук (изобутилен-изопреновый сополимер)
Этилен-пропиленовый (этилен-пропиленовый сополимер)
Бутадиен-нитрильный (бутадиен-акрилонитрильный сополимер)
Хлоропреновый (поли-2-хлорбутадиен)
Силоксановый
Фторкаучуки
Тиоколы.
Наиболее массовое применение каучуков — это производство резин для автомобильных, авиационных и велосипедных шин.
ответ:
) плотность раствора 1,615 г/мл. значит, в 2 л = 2000 мл будет
2000*1,615 = 3230 г раствора.
концентрация раствора составляет 70%, значит, в нем
3230*0,7 = 2261 г кислоты.
молярная масса серной кислоты
m(h2so4) = 2*1 + 32 + 4*16 = 98 г.
значит, 2261 г = 2261/98 ~ 23 моля
молярная концентрация в 2 л раствора составляет
23/2 = 11,5 моль/л
2) масса раствора составляем 25 + 250 = 275 г.
процентная концентрация составляет 25/275 = 0, = 9,09%
3) решаем по той же схеме, как номер 1.
молярная масса фосфорной кислоты
m(h3po4) = 3*1 + 35,5 + 4*16 = 102,5 г
поэтому 32 г = 32/102,5 ~ 0,3122 моля
молярная концентрация в 250 мл = 1/4 л равна
0,3122*4 = 1,2488 моль/л
4) в 100 мл = 0,1 л 1 м раствора содержится 0,1 моля вещества.
добавляем x л 0,1 м раствора, то есть 0,1x моля.
и получаем 0,1 + 0,1x моля на 0,1 + x л вещества.
и это должен быть 0,2 м раствор, то есть
0,1 + 0,1x = 0,2*(0,1 + x)
1 + x = 2(0,1 + x) = 0,2 + 2x
x = 0,8 л = 800 мл.
5) есть 500 мл = 0,5 л 40% раствора naoh, то есть
0,5*0,4 = 0,2 л гидроксида натрия
нам нужно получить 10% раствор, то есть 2 л раствора.
нужно добавить 1,5 л воды.
только я не понял, причем тут плотность раствора naoh.
так что возможно, это неправильное решение.
6) уравнение реакции
hcl + naoh = nacl + h2o
количество hcl и naoh в молях одинаково.
молярные массы
m(hcl) = 1 + 35,5 = 36,5 г, m(naoh) = 23 + 16 + 1 = 40 г
значит, отношение масс веществ в реакции составляет 36,5 : 40
у нас 200 мл = 1/5 л 0,1 m раствора naoh, то есть
40*0,1/5 = 4/5 = 0,8 г гидроксида натрия.
значит, нам нужно
0,8*36,5/40 = 0,73 г hcl.
7) молярная масса воды
m(h2o) = 2*1 + 16 = 18 г.
значит, в 3,6 кг = 3600 г воды содержится
3600/18 = 200 моль
молярная доля соли в растворе составляет
0,4/200 = 0,002
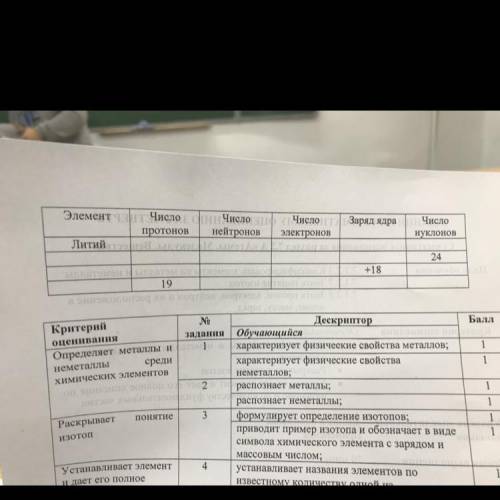
литий
протоны-3
нейтроны-3
электроны-3
заряд ядра-3
Объяснение:
науклоны я не знаю