1)m(KCl)=m (р-ра)*W (KCl)/100%= 500 г*14% /100%=70 г
m(Н2О)=m (р-ра)- m(KCl)= 500 г-70 г=430 г
2)400/100=4г
масса NaCl=4 * 11,7=46,8 грамм
3)Пусть 100г - 100%, тогда Хг - 5%
100г/100%=х/5%
х=100*5/100
х=5г
нужно 5г хлорида калия.
4)задача на картинке
5)Находим массу бензола (масса=объем*плотность): 170 мл * 0,88 г/мл =149,6 г Суммарная масса полученного раствора серы в бензоле составляет: 149,6 г + 1,8 г = 151,4 г. Находим массовую долю серы в растворе: 1,8 г/151,4 г = 0,0119 (или 1,19%) ответ: массовая доля серы в растворе составляет 0,0119 (или 1,19%)
7)w=m остатка/m раствора=12/(80*1.1)=0.1(36)=13.64%
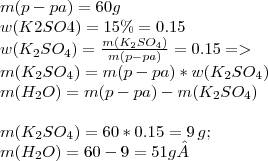
1) 1
2) 1
3) 1
4) 2
5) 3
6) 4
7)2
8) 1
9) 1
10) FeO + 4HNO₃ = Fe(NO₃)₃ + NO₂ + 2H₂O
11) нет вариантов
12) нет вариантов
13) Верно
А. Ионы тяжёлых металлов, содержащего соединения свинца, отрицательно сказывается на состоянии окружающей среды и здоровье людей.
15) 2
Часть 2
Б1
1) строение внешнего электронного слоя соответствует формуле nS²
2) увеличивается число неспаренных электронов в атоме - нет
3) высшие гидроксиды проявляют свойства сильных оснований - да
4) восстановительные свойства усиливаются при уменьшении заряда ядра - нет
5) ослабевают металлические свойства при увеличении порядкового номера - нет
Б2) 2,4
Б3) А2,Б4,В5
А5, Б4, В3
а) m(Cu) = 114kg
m(Zn) = 86kg
w(Cu) = 114/(114+86) = 57%
w(Zn) = 86/(114+86) = 43%
Объяснение: