
Объяснение:
1) Fe + 2HCl → FeCl2 + H2 (хлорид железа (II), водород; реакция замещения).
2) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl (нерастворимые основания получаются реакция их солей с щелочами; гидроксид железа (II), хлорид натрия; реакция обмена, реакция идет, так как образуется осадок в виде гидроксида железа (II)).
3) Fe(OH)2 + H2SO4 → FeSO4 + 2H2O (сульфат железа (II); реакция обмена, реакция идет, так как образуется слабый электролит в виде воды).
4) FeSO4 + BaCl2 → FeCl2 + BaSO4 (хлорид железа (II), сульфат бария; реакция обмена, реакция идет, так как образуется осадок в виде сульфата бария).
При взаимодействии водорода с оксидом хрома (Ⅲ) образуется хром и вода (при сильном нагревании).
Уравнение реакции —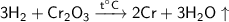 .
.
Коэффициент перед водородом (H₂) - 3, коэффициент перед оксидом хрома (Ⅲ) (Cr₂O₃) - 1, коэффициент перед хромом (Cr) - 3, коэффициент перед водой (H₂O) - 3.
Последовательность коэффициентов для предложенного уравнения реакции — 3, 1, 2, 3. Это ответ.