Для предотвращения гидролиза солей железа(III) можно использовать ионов железа(III) к образованию устойчивых комплексных соединений. Ион железа(III) образует прочные комплексы с щавелевой, винной, лимонной кислотами и с этилендиаминтетра-уксусной кислотой.- Большое число комплексов железо (III) образует с галогенид-ионами типа [Fer4]-, наиболее устойчивыми из которых являются фторидные комплексы. Ниже приведены константы устойчивости некоторых комплексов железа(III) при 25°С:
Реактивы 1
Хлорид железа(III), 1%-ный раствор 0,1 н. по хлористоводо- ]
родной кислоте. |
Винная кислота, 10%-ный раствор. J
Аммиак, 25%-ный раствор. 1
Хлористоводородная кислота, 6 М раствор. |
Выполнение опыта. В цилиндр поместить 30 мл раствора хлорида железа, разбавить до 350 мл водой и добавить 50 мл 6 М раствора хлористоводородной кислоты. На лекции обратить внимание слушателей на зелено-желтый цвет раствора вследствие образования ионов ; [FeCUh". Разлить раствор в два цилиндра. В первый до- , бавить 50 мл раствора аммиака, выпадает красно-бурый j хлопьевидный осадок гидрата окиси железа. Во второй I цилиндр добавить 50 мл раствора винной кислоты, раствор окрашивается в желтый цвет вследствие образования комплексных ионов. Добавить 50 мл раствора аммиака, осадка не образуется.
Примечание. Вместо винной кислоты можно использовать щавелевую, лимонную или кислоты или фторнд аммония.
Алгоритм написания уравнений гидролиза
1. Определяем тип гидролиза. Необходимо написать уравнение диссоциации соли.
Гидролиз сульфата меди(II): CuSO4 = Cu2+ + SO42–
Соль образована катионом слабого основания и анионом сильной кислоты. Гидролиз по катиону.
2. Записываем ионное уравнение гидролиза, определяем среду:
Cu2+ + HOH CuOH+ + H+;
образуется катион гидроксомеди(II) и ион водорода, среда кислая
3. Составляем молекулярное уравнение. Из положительных и отрицательных частиц находящихся в растворе, записываются нейтральные частицы, существующие только на бумаге. В данном случае из CuOH+ SO42– составляем (CuOH)2SO4. Для уравнивания числа ионов меди необходимо перед сульфатом меди поставить коэффициент два. Получаем:
2CuSO4 + 2H2O (CuOH)2SO4 + H2SO4
Продукт реакции относится к группе основных солей: сульфат гидроксомеди(II).
Дано : n(CO) = 2 моль.
Найти : V(CO₂) = ?
Уравнение реакции -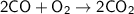 .
.
По уравнению реакции - n(CO) = n(CO₂) = 2 моль.
V(CO₂) = n(CO₂)*Vₘ = 2 моль*22,4 л/моль = 44,8 л.
ответ : 44,8 л.