Cu - медь.
Объяснение:
При разложении гидроксида двухвалентного металла массой 19.6 г, образуется оксид двухвалентного металла массой 16 г. Определите металл. Решите с уравнения реакции.
Металл обозначим как - «Me», тогда общая формула будет : Me(OH)2, так как OH-группа является одновалентной.
Схема разложения: Me(OH)2 —> MeO + H2O
Дано:
m(MeOH)2 = 19.6 г
m(MeO) = 16 г.
m(H2O) = 19.6 - 16 = 3.6 грамм
Помним, что сумма реагентов и образующихся продуктов должна быть равной !
И так, нам известно, что воды образуется 3.6 грамм по задаче, а по реакции 18 грамм, из этого следует, что:
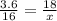
x= 80
80 грамм молекулярная масса оксида двухвалентного металла (MeO)
80-16(кислород в составе MeO) = 64 г
64 г это атомная масса Меди.
Если будут вопросы, отвечу с удовольствием в комментариях.
Объяснение:
39. Раствор какой концентрации можно получить при смешивании 20% -ного и 60 % -ного растворов с одинаковыми массами.
Если массы растворов одинаковы, например по 100 г то подобная задача решается просто:
20% + 60%
= 40%
2
Если же массы растворов различаются, то необходимо первоначально найти массы растворимого вещества в каждом растворе, а затем сумму этих масс разделить на суммарную массу растворов.
Например, смешали 150 г 8% раствора КОН и 200 г 12% раствора КОН. Найти массовую долю растворенного вещества во вновь полученном растворе.
1. Находим массу КОН в первом растворе:
150 г × 0,08 = 12 г КОН
2. Находим массу КОН во втором растворе:
200 г × 0,12 = 24 г КОН
3. Найдем суммарную массу КОН:
12 г + 24 г = 36 г КОН
4. Найдем суммарную массу растворов:
150 г + 200 г = 350 г
5. Вычислим массовую долю КОН в полученном растворе
ω(КОН) = 36 г /350 г = 0,1028 х 100% = 10,28%
2-Ca(OH)2
3-CO2 и CuCl2
4-AgNO3