У неорганічній хімії важливу роль відіграють хімічні реакції. Найважливішими з них є Кислотно-основні реакції та Окисно-відновні реакції. Як правило ці реакції є рівноважними та з високою ентальпією. Через це хімічні реакції у неорганічній хімії є дуже швидкими і з високим виходом продуктів реакції. На противагу, хімічні реакції у органічній хімії є часто повільними і не завжди з високим виходом продуктів реакції.
У процесі окисно-відновної реакції відновник віддає електрони, тобто окиснюється; окисник приєднує електрони, тобто відновлюється. Причому будь-яка окисно-відновна реакція є єдність двох протилежних перетворень — окиснення та відновлення, що відбуваються одночасно та без відриву одне від одного. Типовими і найпростішими окисно-відновними реакціями є утворення сполук з окремих елементів: наприклад утворення води з кисню і водню, чи корозія металів коли, наприклад, Ферум реагує з киснем з утворенням оксидів.
У кислотно-основних реакціях відбувається перенесення протону. Кислота передає основі протон. При цих реакціях в основному утворюється вода і сіль. Наприклад:
{\displaystyle \mathrm {H_{3}O_{(aq)}^{+}+Cl_{(aq)}^{-}+Na_{(aq)}^{+}+OH_{(aq)}^{-}\longrightarrow \ Na_{(aq)}^{+}+Cl_{(aq)}^{-}+2\ H_{2}O} }{\displaystyle \mathrm {H_{3}O_{(aq)}^{+}+Cl_{(aq)}^{-}+Na_{(aq)}^{+}+OH_{(aq)}^{-}\longrightarrow \ Na_{(aq)}^{+}+Cl_{(aq)}^{-}+2\ H_{2}O} }
Хлоридна кислота + Гідроксид натрію реагують у водному розчині з утворенням Хлориду натрію та води.
Такі реакції протікають також швидко і легко контролюються за до індикатора, що дозволяє використовувати їх у аналітичній хімії.
Утворення нерозчинних чи газоподібних продуктів реакції є їх важливою рушійною силою. При цьому ці продукти залишають зону реакції і при цьому зрушують рівновагу у сторону утворення цих продуктів так, що реакція протікає до кінця. Так наприклад при реакції розчинів хлориду барію та сульфату натрію, утворюється важкорозчинний сульфат барію. При його відфільтруванні у розчині, що залишився не знаходять більше йонів барію.
{\displaystyle \mathrm {BaCl_{2}+Na_{2}SO_{4}\longrightarrow BaSO_{4}+2\ NaCl} }{\displaystyle \mathrm {BaCl_{2}+Na_{2}SO_{4}\longrightarrow BaSO_{4}+2\ NaCl} }
Реакції такого типу відіграють також важливу роль у аналітичній хімії. Різномнітні неорганічні сполуки можуть при високих температурах розкладатися з виділенням газів. Так при нагріванні карбонат кальцію, не плавлячись, розкладається з утворенням оксиду кальцію і діоксиду вуглецю:
{\displaystyle \mathrm {CaCO_{3}\longrightarrow CaO+CO_{2}} }{\displaystyle \mathrm {CaCO_{3}\longrightarrow CaO+CO_{2}} }↑
ответ: 52.8грамм
Объяснение:
Есть известь негашеная - CaO (оксид кальция II)
А есть гашеная - Ca(OH)2 (гидроксид кальция)
Также есть известь как материал - CaO и MgO
Процесс нагревания означает реакцию разложения, то есть в выходе будут только те атомы, которые были в исходных продуктах. А во всех предложенных известях нет углерода, поэтому углекислый раз в принципе не образуется. Поэтому задача нерешаема.
НО есть известь воздушная или же мел - CaCO3, который уже подходит и делает реакцию
CaCO3→СаО+СО2↑
Если идти так, то задача крайне тривиальна, так как количество молей углекислого газа и извести совпадает. То есть n(CaCO3)=n(CO2)
n(CaCO3)=m(CaCO3)/M(CaCO3)
m(CO2)=n(CO2)*M(CO2)=n(CaCO3)*M(CO2)=m(CaCO3)/M(CaCO3)*M(CO2)=
=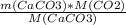 =
= =52.8 г.
=52.8 г.
Дано:
m(CaCO3)=120г.
Найти: m(CO2)
Решение расписал