1.Сначала найдем через относительную плотность молекулярную массу вещества:
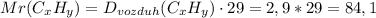
2.Теперь найдем массы Углерода и Водорода за массами продуктов горения:
а)масса Углерода:
44 г углекислого газа содержит 12 г Углерода,а
6,6 г________________________х г, откуда х=6,6*12/44=1,8 г
б)масса Водорода:
18 г воды содержит 2 г Водорода,а
2,7 г_____________у г, откуда у=2*2,7/18=0,3 г
3.Если сложить полученные массы,то получится 2,1 г,значит это углеводород.так как действительно состоит из атомов Водорода и Углерода(если бы этой суммы не хватало бы,то разница между массой вещества и этими двумя массами элементов,дало бы массу третьего элемента,Кислорода,это на будущее).Теперь поделив каждую массу элемента на массу всего вещества,получим массовые доли этих элементов:
w(C)=1,8/2,1=0,8571 или 85,71%
w(H)=100% - w(C)=100 - 85,71=14,29%
4.Теперь осталось найти количество атомов каждого из элементов в веществе.Для этого необходимо вспомнить формулу по определению массовой доли элемента в веществе и вывести из нее n:
n(C)=Mr(CxHy)*w(C)/Ar(C)*100%=84,1*85,71/12*100=6
n(H)=Mr(CxHy)*w(H)/Ar(H)*100%=84,1*14,29/1*100=12
Вот и выходит,что формула углеводорода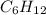 -это гексен - представитель непредельных углеводородов ряда этилена,так как подходит под общую формулу
-это гексен - представитель непредельных углеводородов ряда этилена,так как подходит под общую формулу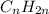
Для того, чтобы уменьшить объем в два раза, надо в два раза увеличить давление. В 16 раз увеличится, потому что при этом концентрации водорода и азота возрастут в два раза, а водород вступает в реакцию с коэффициентом 3... Именно поэтому синтез аммиака проводят при высоком давлении.
Но гораздо интереснее вопрос, а почему же этот синтез проводят еще и при весьма высокой температуре, если реакция образования аммиака - экзотермическая и повышение температуры сдвигает равновесие в сторону исходных веществ? Так зачем же повышать температуру? Это же невыгодно с точки зрения смещения равновесия? Почему не проводить реакцию при температуре, к примеру, окружающей среды? Вот если сможете ПРАВИЛЬНО ответить на ЭТОТ ВОПРОС - то это будет означать, что вы НЕМНОЖКО стали ПОНИМАТЬ химию...