Дано:
m(технического CaCO₃)=800г.
ω%(примесей в CaCO₃ )=12,%
Vm=22,4л./моль
V(CO₂)-?
1. Определим массу чистого карбоната кальция:
m(CaCO₃)=m(технического CaCO₃)xω%(примесей в CaCO₃ )÷100%
m(CaCO₃)=800г.×12,%÷100%=96г.
2. Определим молярную массу карбоната кальция и его количество вещества в 96г:
M(CaCO₃)=100г./моль
n₁(CaCO₃)=96г÷100г./моль=0,96моль
3. Запишем уравнение реакции разложения карбоната кальция:
CaCO₃ = CaO + CO₂
по уравнению реакции:
n(CaCO₃)=n(CO₂)=1моль
по условию задачи:
n₁(CaCO₃)=n₁(CO₂)=0,96моль
4. Определим объем оксида углерода(IV) :
n₁(CO₂)=0,96моль
V(CO₂)=n₁(CO₂)x22,4л./моль
V(CO₂)=0,96мольх22,4л./моль=21,5л.
5. ответ: при разложении 800г. технического карбоната кальция с массовой долей примесей 12% образовалось 21,5л. углекислого газа (оксида углерода(IV).
Уравнение реакции( один из вариантов):
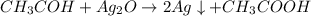
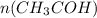 = 4,4 / 44= 0,1 моль
= 4,4 / 44= 0,1 моль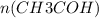 =
= 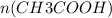 = 0,1 моль
= 0,1 моль
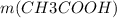 =
= 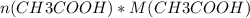 = 0,1 * 60 = 6 г.
= 0,1 * 60 = 6 г.
Чтобы расчитать выход продукта, нам нужно узнать сколько теоретически должно было выделиться продукта( "на бумаге").
Воспользуемся известной массой уксусного альдегида и найдём, сколько этого самого альдегида вступило в реакцию:
n( количество вещества) = m( масса) / M( молярная масса) - общая формула
Из уравнения реакции видно, что коэффициент перед уксусным альдегидом равен коэффициенту перед уксусной кислотой, т.е.
Теперь, пользуясь уже знакомой формулой n( количество вещества) = m( масса) / M( молярная масса), мы можем найти массу ( теоретическую) уксусной кислоты:
Выход продукта расчитываем по формуле:
w = m( практ) / m( теор) * 100% = 90%
ответ: выход продукта составил 90%.