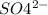
Дано: Решение:
m(Al2O3)=20,4 г. 4Al+3O2=2 Al2O3 -уравнение реакции
M(Al2O3)=102г/моль 1)n=m/M
n(Al2O3)=20,4/102=0,2 моль
Найти: m(Al) 2)n(Al2O3): n(Al)=2 : 4 => n(Al)=0,4 моль
3)m=n*M
m(Al)=0,4*27=10,8 г.
Объяснение:
Расставить коэффициенты в уравнениях реакций, для окислительно-восстановительных реакций записать электронный баланс, для реакции обмена – ионные уравнения (задание для 1 и 2 варианта):
-2 0 -2 +4
a)2CuS + 3O2 =2CuO + 2SO2
S(-2) - 6e = S(+4) окисление, S(-2) - восстановитель ║ 2
O2(0) +4e = 2O(-2) восстановление, О2 - окислитель ║ 3
-1 0 -1 0
б)2KBr + Cl2 = 2KCl +Br2
2Br(-) - 2e = Br2(0) окисление, 2Br(-) - восстановитель║1
Cl2(0) +2e = 2Cl(-) восстановление, Cl2 - окислитель ║1
в) 2HNO3 + Zn(OH)2 = Zn(NO3)2 + 2H2O
2H+ + 2NO3 - + Zn(OH)2 = Zn2+ + 2NO3 - + 2H2O
2H+ + Zn(OH)2 = Zn2+ + 2H2O
0 0 +1 -2
г) 4Li + O2 = 2Li2O
Li(0) - 1e = Li+ окисление, Li - восстановитель ║4
O2 +4e = 2O(-2) восстановление, О2 - окислитель ║ 1
Объяснение:
следовательно в растворе Al, содержится больше всего а) Al^+3