Молекулярное:
S + 2K -> K2S
Полное ионное:
S + 2K -> 2K(+)+S(-2)
Сокращенное ионное будет выглядеть таким же образом, что полное.
Молекулярное:
K2S + 2HCI -> 2KCI + H2S⬆️
Полное ионное:
2K(+)+S(-2) + 2H(+)+2CI(-) -> 2K(+)+2CI(-) + H2S⬆️
Сокращенное ионное:
S(-2) + 2H(+) -> H2S⬆️
Молекулярное:
2H2S + 3O2 -> 2H2O + 2SO2⬆️
Полное и сокращенное ионное будут выглядеть таким же образом, что молекулярное.
С расставленными степенями окисления:
2Н2(+)S(-2) + 3O2(0) -> 2H2(+)O(-2) + 2S(+4)O2(-2)
S(-2)--(-6ē)-->S(+4) | 6 | ×2
- восстановитель(отдает электроны), процесс окисления
O2(0)--(+4ē)-->2O(-2)|4|×3
- окислитель(получает электроны), процесс восстановления.
Молекулярное:
2SO2 + O2 -> 2SO3
Полное и сокращенное ионное будут выглядеть таким же образом, что молекулярное.
Молекулярное:
SO3 + NaOH -> NaHSO4
Полное ионное:
SO3 + Na(+)+OH(-) -> Na(+)+HSO4(-)
Сокращенное ионное:
SO3 + OH(-) -> HSO4(-)
Молекулярное:
NaHSO4 + NaHCO3 -> Na2SO4 + H2O + CO2⬆️
Полное ионное:
Na(+)+HSO4(-) + Na(+)+HCO3(-) -> 2Na(+)+SO4(-2) + H2O + CO2⬆️
Сокращенное ионное:
HSO4(-) + HCO3(-) -> SO4(-2) + H2O + CO2⬆️
1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
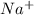

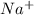
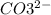

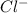
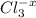


BaO + H2O = Ba(OH)2
Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O