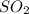
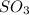
П р и м е р 1. Какие массы соли и воды требуются для приготовления 500 г 3 % раствора?
Д а н о :
т = 500 г
ω = 3 %
т ( х )= ?
т (Н20) = ?
Р е ш е н и е
т (х ) = m∗ω
100
; т ( х )=500 г∗3
100
= 1 5 г
Чтобы рассчитать массу воды, нужно из
общей массы раствора вычесть массу
растворенного вещества,
т (Н20) = т — т (х ); т (Н20) = 500 г —
15 г = 485 г.
ответ: для приготовления требуемого раствора следует взять 15 г соли и 485 г
воды.
9. Сульфат магния в виде раствора с массовой долей 25 % применяется при
гипертонической болезни. Какая масса этой соли необходима для приготовления 300 г
раствора?
10. Какие массы сахара и воды требуются для приготовления 250 г 10 % раствора?'
11. Раствор хлорида бария используется для осаждения из него сульфата бария,
используемого в рентгеноскопии. Какая масса хлорида бария требуется для
приготовления 50 г 0,5 % раствора?
12. Какую массу 5% раствора можно приготовить из 25 г сульфата меди (II). Какая
масса воды для этого необходима?
В лабораторной практике часто приходится иметь дело с кристаллогидратами —
солями, содержащими кристаллизационную воду, например, CuS04 • 5Н20, FeS04 • 7Н20
и т. д. При приготовлении растворов с использованием таких солей при расчете следует
учитывать кристаллизационную воду.
П р и м е р 2. Какую массу кристаллогидрата медного купороса CuS04 • 5Н20 надо
взять, чтобы получить
200 г 5 % раствора сульфата меди( I I ) ? Какая масса воды для этого потребуется?
Д а н о :
M (CuS04-5H20) = 250 г/моль
m = 200 г
ω = 5 %
М (CuS04) = 160 г/моль
Р е ш е н и е
Сначала находим массу сульфата меди (II), необходимую для приготовления раствора по формуле:
т ( x ) = m∗ω
100
;
т ( Сu S O4 )=200 г∗5
100
= 1 0 г ( Сu S O4 )
т (CuS04) = ?
т (CuS04*5H20) = ?
т (Н20) = ?
Далее следует определить массу кристаллогидрата
CuS04*5H20. При этом имеем в виду, что сульфат
меди (II) CuS04 входит в состав кристаллогидрата в
строго определенном массовом соотношении.
Чтобы его найти, надо вычислить массы:
т (CuS04-5H20) = 250 г/моль*1 моль = 250 г;
т (CuS04) = 160 г/моль*1 моль = 160 г.
(Расчет показывает, что масса в граммах любого
вещества, взятого в количестве 1 моль, численно
равна молярной массе, поэтому этот вс расчет не обязательно всякий раз записывать при
решении задачи. Важно помнить, что молярная масса
и масса — это разные величины, имеющие разное
наименование, и их нельзя путать)
Из пропорции видно, что
в 250 г CuS04-5H20 — 160 г CuS04
в m г CuS04-5H20 — 10 г CuS04
т (CuS04*5H20) =
250 г∗5 г
160 г
=1 5 , 6 г ( Сu S O4 *5H20)
Мы выяснили, что для приготовления 200 г
раствора CuS04 требуется 15,6 г медного купороса.
Определяем необходимую массу воды:
т (Н20) = 200 г — 15,6 г = 184,4 г.
ответ: для приготовления 5 % раствора CuS04
необходимо 15,6 г кристаллогидрата и 184,4 г воды.
13. Сульфат натрия используется в медицине как слабительное. Какая масса
кристаллогидрата Na2SO4*10H2O понадобится для приготовления 2 кг
Объяснение:
1) а) 1. 2Mg + O₂ -> 2MgO
2. MgO + CO₂ -> MgCO₃
3. MgCO₃ + 2NaOH -> Mg(OH)₂ + Na₂CO₃
4. Mg(OH)₂ -> MgO + H₂O
5. MgO + C -> CO + Mg
б) 1. 2N₂ + 5O₂ -> 2N₂O₅
2. N₂O₅ + H₂O -> 2HNO₃
3.8 HNO₃ + 3Mg -> 3Mg(NO₃)₂ + 4H₂O + 2NO
2) Дано:
m(HNO₃) = 126г
Найти:
V(N₂O₅) - ?
Записываем уравнение реакции:
N₂O₅ + H₂O -> 2HNO₃
Находим количество вещества азотной кислоты:
M(HNO₃) = 1 + 14 + 3 × 16 = 63г/моль
n(HNO₃) = 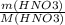 =
= 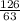 = 2 моль
= 2 моль
Находим количество вещества оксида азота:
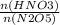 =
= 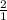 => n(N₂O₅) =
=> n(N₂O₅) = 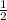 n(HNO₃) = 2 × 0,5 = 1 моль
n(HNO₃) = 2 × 0,5 = 1 моль
Находим Объём оксида азота:
V(N₂O₅) = n(N₂O₅) × Vm = 1 моль × 22,4 л/моль = 22,4 л
ответ: 22,4 л
Объяснение:
оксид серы VI SO3