гидроксид натрия будет реагировать с:
А)кислотами
HNO3 + NaOH = NaNO3 + H2O
б) с солью, если образуется осадок
NaOH + CuSO4 = Cu(OH)2 (осадок) + Н2SO4
Г)с кислотными оксидами
NaOH + CO2 = NaCO3 + H2O
6NaOH+P2O5=2Na3PO4 + 3H2O
Сu + 2АgNO3 = Сu(NО3)2 + 2Аg. Cначала определим возможное теоретическое изменение массы стержня в соответствии с уравнением (1): растворение 1 моль меди привело бы к увеличению массы на152 г (2•108 – 64 = 152), а растворение х моль меди – к увеличению массы реально на31,2 г.
х = 31,2•1/152 = 0,205 моль,
n(Сu) = 0,205 моль, n(Аg) = 0,41 моль.
Эти данные позволяют нам вычислить массы растворившейся меди и выделившегося серебра:
m(Сu) = 0,205•64 =13,12 г,
m(Ag) = 0,41•108 =44,34 г.
В итоге на стержне оказалось:
m(Сu) = 140 – 13,2 =126,88 г,
n(Сu) = 126,88/64 = 1,98 моль,
m(Ag) =44,34 г, n(Ag) = 44,34/108 = 0,41 моль.
И медь, и серебро будут взаимодействовать с достаточным количеством азотной кислоты в соответствии с уравнениями
0,41моль х моль
3Ag + 4HNO3=3AgNO3+NO+2H2O
1,98 моль у моль
3Cu + 8HNO3=3Cu(NO3)2+ 2NO+4H2O
х + у = 0,55 + 5,28 = 5,83 моль
или по массе:
m(HNO3) = 63•5,83 = 367,29 г.
Теперь можно определить массу необходимой для этой реакции 32%-й азотной кислоты, а затем и объем этой кислоты:
m(32%-й HNO3) = m(100%-й HNO3)•100% / = 367,29•100/32 = 1147,78 г,
V(32%-й HNO3) = 1147,78/1,2 = 956,48 мл.
1680 г х л
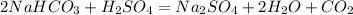
168 г 22,4 л
1. Сначала переведем объем раствора в массу через плотность,учитывая,что 20 л - это 20 000 мл или 20 000 см в кубе:
m(раствора)=V*р(ро)=20 000* 1,05=21 000 г
2. Теперь определим чистую массу гидрокарбоната в растворе,учитывая,что 8% - это 0,08(но без %):
m(NaHCO3)=m(раствора)*w(NaHCO3)=21 000*0,08=1680 г
3. А теперь,подставив эту массу в уравнение,решаем как обычно с пропорции:
при взаимодействии 168 г гидрокарбоната выделится 22,4 л углекислого газа, а
при -- \\ -- 1680 г_______________________х л, откуда
х=1680*22,4/168=224 л
1)NaOH+HNO3=NaNO3+H2O
2)NaOH+CO2=NaHCO3
3)2NaOH+CuSO4=Cu(OH)2+Na2SO4
4)NaOH+P2O5=Na3Po4+H2O