125 г х г у г
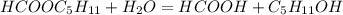
116 г 46 г 88 г
1. Знайдемо масу кислоти:
при взаємодії 116 г естеру утворюється 46 кислоти, а
при -- // -- 125 г__________________х г, звідки
х=125*46/116=приблизно 50 г
2. Тепер обчислимо массу спирту:
при взаємодії 116 г естеру утворюється 88 г спирту, а
при -- // -- 125 г_________________у г, звідки
у=125*88/116=приблизно 95 г
№1
Сa(OH)2+BaF
Ca2SO4
CuCl2+H2
Zn2Co3+H2O
CaS2+H2
Вроде так)