1.
А. 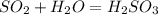
Б. 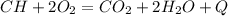
В. 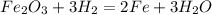
1.
А. 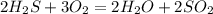
Б. 
В. 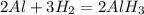
2.
mH2O = 35г
mсоли = 10г
mраствора = mсоли+mводы = 35г+10г = 45г
w = mсоли/mр-ра = 10г/45г*100% = 22,2%
2.
mр-ра = 300г
wсоли = 0,05
mсоли = w*mр-ра = 0,05*300г = 15г
mводы = mр-ра - mсоли = 300-15 = 285г
3.
C -> XH4 -> CO2 -> H2CO3
1. C + 2H2 = CH4 - соединение, обр. метан
2. CH4 + 2O2 = CO2 + 2H2O - разложение, с образованием углекислого газа и воды.
3. CO2 + H2O = H2CO3 - соединение, обр. уголная кислота
3.
Al -> Al2O3 -> Al -> Al(OH)3
1. 4Al + 3O2 = 2Al2O3 - соединение, обр. оксид алюминия.
2. 2Al2O3 --эл. ток--> 4Al + 3O2 - разложение, обр. алюминий и кислород
3. 2Al + 6H2O = 2Al(OH)3 + 3H2 - замещение, обр. гидроксид алюминия и водород.
2.Из этих двух веществ будет обладать максимальным поверхностным натяжением тот раствор, в котором силы взаимодействия молекул ПИАВ и растворителя больше. Оценим это взаимодействие через энтальпию гидратации ионов:
для NaOH: стандартная энтальпия гидратации Na+=-423 кдж/моль, ОН-=-510,45 кдж/моль
для H2SO4: стандартная энтальпия гидратации Н+=-1129 кдж/моль
стандартная энтальпия гидратации SO42-=-1129 кдж,моль
3. Поскольку тепловые эффекты реакции гидратации ионов, входящих в состав серной кислоты, больше, чем у ионов, входящих в состав щелочи, силы взаимодействия молекул кислоты и воды больше.
т.о., раствор серной кислоты будет обладать максимальныи поверхностным натяжением.