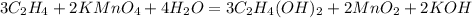(Реакция протекает под действием платинового катализатора)
(Реакция протекает под действием платинового катализатора)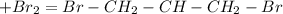
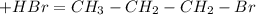
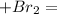 циклопентан
циклопентан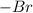
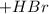
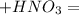 циклогексан
циклогексан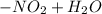 (Реакция протекает при температуре 120°С)
(Реакция протекает при температуре 120°С)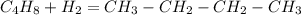 (Реакция протекает под действием платинового катализатора)
(Реакция протекает под действием платинового катализатора)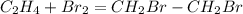
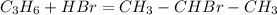
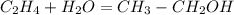 (Реакция протекает под действием фосфорной кислотой)
(Реакция протекает под действием фосфорной кислотой)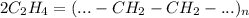 (Реакция протекает по свободнорадикальному механизму)
(Реакция протекает по свободнорадикальному механизму)