Відповідь:Этанамин - C2H5NH2
Этан - С2Н6
С хлоридной кислотой в склянке реагирует только этанамин:
C2H5NH2 + HCl = [C2H5NH3]Cl
(реакция для решения задачи не нужна)
Следовательно, при пропускании газовой смеси, на выходе получаем чистый этан; этанамин - поглощается.
Делаем вывод, что увеличение массы склянки связано с поглощением этанамина, т.е. масса этанамина в исходной смеси - 9 г.
По условию задачи массовая доля этана в исходной смеси - 25 %. Тогда этанамина - 75 %.
Найдем массу этана по пропорции:
m(С2Н6) - 25 %
9 г (m(C2H5NH2)) - 75 %
Отсюда m(С2Н6) = 9*25%/75% = 3 г.
Массы газов мы знаем. Теперь пересчитываем массы в объем при н.у. по формуле:
V = Vm*m/M
Vm - молярный объем, 22,4 л/моль
М - молярная масса вещества
Для этанамина
V = 22,4*9/45 = 4,48 л = 4480 мл
для этана
V = 22,4*3/30 = 2,24 л = 2240 мл
Объем исходной газовой смеси равен 4480+2240 = 6720 мл
Пояснення:
Так, сначала условные обозначения:
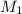 - масса исходного раствора
- масса исходного раствора
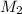 - масса получившегося раствора
- масса получившегося раствора
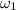 - массовая доля вещества впервом растворе
- массовая доля вещества впервом растворе
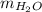 - масса добавленной воды
- масса добавленной воды
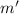 - масса добавленного вещества
- масса добавленного вещества
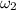 - массовая доля получившегося вещества
- массовая доля получившегося вещества
1 - Определим на сколько грамм увеличили массу раствора:
250 + 32 = 285г - мы сложили массу добавленной воды и массу добавленной соли
2 - Рассчитаем массу получившегося раствора:
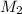 =
= 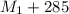 = 600 грамм
= 600 грамм
3 - Определим массу вещества в растворе:
m =  = 315*0,15 =47,25г
= 315*0,15 =47,25г
4 - Рассчитаем на сколько стало вещества в полученном растворе, ведь помимо воды, мы добаваляем и вещества:
m(получ) = 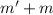 = 35г + 47,25г = 82,25г
= 35г + 47,25г = 82,25г
5 - Считаем массовую долю: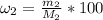 = 82,25/600*100% = 13,7%
= 82,25/600*100% = 13,7%
Cu(NO₃)₂ + 2KOH = Cu(OH)₂ + 2KNO₃
Cu(OH)₂ + H₂SO₄ = CuSO₄ + 2H₂O
2CuSO₄ + 2NH₄OH = (СuOH)₂SO₄ + (NH₄)₂SO₄
(СuOH)₂SO₄ + H₂SO₄ = 2CuSO₄ + 2H₂O