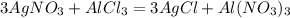
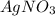 ) = 170 г/моль
) = 170 г/моль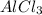 ) = 132 г/моль
) = 132 г/моль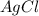 ) = 143 г/моль
) = 143 г/моль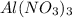 ) = 213 г/моль
) = 213 г/моль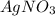 ) = 23,8/(170 * 3) = 0,047 моль
) = 23,8/(170 * 3) = 0,047 моль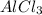 ) = 5,34/132 = 0,040 моль
) = 5,34/132 = 0,040 моль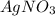 - избытке, значит расчет ведем по
- избытке, значит расчет ведем по 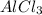
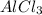
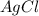 ) = (5,34 * 143 * 3)/132 = 17,35 г
) = (5,34 * 143 * 3)/132 = 17,35 г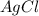 и
и 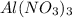 - продукты реакции и не прореагировавший
- продукты реакции и не прореагировавший 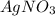
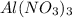 ) = 5,34 * 213 / 132 = 8,62 г
) = 5,34 * 213 / 132 = 8,62 г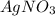 ) = 170 * 3 * 5,34 / 132 = 20,63 г - израсходовалось в ходе реакции
) = 170 * 3 * 5,34 / 132 = 20,63 г - израсходовалось в ходе реакции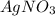 ) = 23,8 - 20,63 = 3,17 г - не прореагировало
) = 23,8 - 20,63 = 3,17 г - не прореагировало
n2(NaOH) = c2*V2 = 6*0,15 = 0,9 моль
n(NaOH) = n1(NaOH) + n2(NaOH) = 1 + 0,9 = 1,9 моль
V раствора = V1+V2 = 0,25 + 0,15 = 0,4 л
c = = 4,75 моль/л
ответ: 4,75 моль/л