1. При прибавлении к раствору цитрата избытка известковой воды на холоду осадка не образуется. При нагревании же выпадает хлопьевидный осадок цитрата калия, при охлаждении (в закрытой колбе) вновь растворяющийся.
2. Нагревают 5 мл 1%-ного раствора лимонной кислоты с 1 мл реактива Дениже (5 г окиси ртути растворяют в смеси 20 мл концентрированной серной кислоты и 100 мл воды при нагревании до кипения) и прибавляют несколько капель 2%-ного раствора пер-манганата калия. Жидкость обесцвечивается и выпадает белый кристаллический осадок:
Промытый осадок растворяется в растворе хлорида натрия с образованием хлорида ртути и ацетон-дикарбоновой кислоты, которая с хлоридом железа дает малиново-красное окрашивание. 3. Реакция образования пентабромацетона
К водному раствору лимонной кислоты или цитрата в очень разбавленной серной или азотной кислоте (но не соляной) прибавляют
2-5 капель 0,1 н. раствора перманганата калия и нагревают в течение непродолжительного времени до 30-40° (только не кипятить!). Как только раствор побуреет или помутнеет от незначительного выделения двуокиси марганца, прибавляют 1-2 капли раствора ок-салата аммония и 1 мл 10%-ной серной кислоты, при этом жидкость становится прозрачной. Затем прибавляют несколько капель бромной воды. При этом выделяется кристаллический осадок пента-бромацетона.1
4.Глюкоза даёт синее окрашивание с свежеприготовленным Сu(OH)2. Даёт реакцию серебрянного зеркала с Ag(NH3)2OH/
1. Тип химической связи в соединении Н2О: в) ковалентная полярная
2. Наиболее электроотрицательный химический элемент: б) Cl
3. Заряд иона кальция: а) 2+
4. Завершенный внешний электронный слой имеет атом химического элемента: а) Не
5. Число общих электронных пар между атомами в молекуле О2 равно:
б) 2
О=О
6. Ковалентная неполярная связь образуется между:
а) атомами одного неметалла
7. Сущность ионной связи состоит:
а) в электростатическом притяжении между разноименными зарядами
(ионами)
8. Электроотрицательность химических элементов в периодах с увеличением порядкового номера элемента:
а) увеличивается
9. К правильным утверждениям относятся:
а) соединяясь между собой, атомы стремятся к достижению устойчивого состояния
г) между калием и хлором образуется ионная связь
10. В периоде слева направо радиус атома и металлические свойства
соответственно: г) уменьшается и уменьшаются
11. Внешний уровень считается завершенным (кроме водорода и гелия), если на нем:
тогда г) 8 электронов
12. Образование молекулы водорода из атомов, можно изобразить:
г) H • + • H → H •• H
13. В какой молекуле тройная связь? а) N2
14. Выберите элемент с переменной валентностью:
а) Cl
15. При образовании ковалентной полярной связи электронная пара:
г) смещена к более электроотрицательному элементу
16. В каком соединении валентность железа равна III?
в) Fe2O3
17. Ковалентная полярная связь образуется между:
в) различными атомами неметаллов
18. В ряду элементов: Al Si P S: ?????
а) увеличивается число электронных слоев в атомах;
б) усиливаются неметаллические свойства;
в) уменьшается число внешних электронов в атомах;
г) возрастают радиусы атомов.
19. Напишите электронную и электронно-графическую формулы для атома Са.
+20 ) ) ) ) 1s² 2s² 2p⁶ 3s² 3p⁶ 4s₂
2882
Укажите валентность элемента = II.
20. Запишите электронные и графические схемы образования молекулы HCl..
в фото
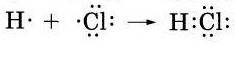
2NaOH + SO3 = Na2SO3 + H2O
реакция не идёт
2NaOH + Mg(NO3)2 = 2NaNO3 + Mg(OH)2