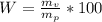
1) Находим молекулярную массу вещества
Mr = D(H2) x Mr(H2) = 15 х 2 = 30.
Определяем, сколько по массе приходится на углерод.
30 - 100%
х - 80%
х = 24
Определяем, сколько по массе приходится на водород
m(H) = 30-24 = 6
Определяем число атомов углерода и водорода в данном веществе.
N(C) = m/Ar = 24/12 = 2 атома
N(H) = m/Ar = 6/1 = 6 атомов
Формула С2Н6 - этан
2)Находим молекулярную массу вещества
Mr = D(воздуха) x Mr(воздуха) = 2,69 х 29 = 78
Определяем, сколько по массе приходится на углерод.
78 - 100%
х - 92,3%
х = 72
Определяем, сколько по массе приходится на водород
m(H) = 78-72 = 6
Определяем число атомов углерода и водорода в данном веществе.
N(C) = m/Ar = 72/12 = 6 атомов
N(H) = m/Ar = 6/1 = 6 атомов
Формула С6Н6- бензол
Объяснение:
ВРОДЕ ПРАВИЛЬНО
наибольшее при реакции магния и кислоты
наименьшее при реакции цинка и кислоты
Объяснение:
Запишем уравнения реакций:
Mg+2HCl=MgCl2+H2
Zn+2HCl=ZnCl2+H2
Исходя из уравнений, количество водорода, синтезируемое в результате первой и второй реакций равно и будет зависеть только от количества металлов (определяем по недостатку), тогда, запишем формулы для количеств Mg и Zn:
1. υ(Mg)=m(Mg)/M(Mg)=m(Mg)/24
2. υ(Zn)=m(Zn)/M(Zn)=m(Zn)/65
т.к. m(Zn)=m(Mg) по условию, пусть m(Zn)=m(Mg)=х, очевидно, что х/24>х/65, следует, что υ(H2)1>υ(H2)2,
тогда и, V(H2)1=υ(H2)1*Vm,
V(H2)2=υ(H2)2*Vm, Vm=const
следует, что: V(H2)1>V(H2)2
массовая доля первого раствора w1= x/15
массовая доля второго раствора (после приливания воды) : w2 = x/115
w1/w2 = x/15 : x/115 = 7.7 раз
Значит, концентрация уменьшится в 7.7 раза
Наверное, так.