Металлам, как простым соединениям (атомам) характерны восстановительные свойства, на последнем слое у них мало электронов и они легко их отдают, например:
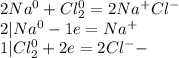
Натрий - восстановитель
Хлор окислитель
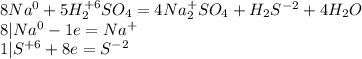
Натрий - восстановитель
Сера - окислитель
Ионам же металлов характерны окислительные свойства, если они меняют свою степень окисления (покидая соединения):
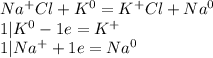
Калий (простое в-во) - восстановитель
Натрий (ион в составе соли) - окислитель
Если металлы не покидают своих соединений, то и степени окисления они зачастую не меняют:
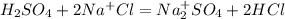
Техническое железо содержит примеси, которые, как правило, выполняют роль катода. Либо, если это углерод, который не передает в раствор положительно заряженных ионов и не имеет заградительного барьера от ионов водорода в кислой среде. Само железо будет служить анодом и подвергаться разрушению.
В химически чистом железе нет примесей, которые образовали бы гальванопару с железом, где бы оно окислялось.
При коррозии технического железа протекают следующие реакции:
Во влажном воздухе
А: Fe – 2e— = Fe2+
K: O2 + 2H2O + 4e— = 4OH—
2Fe + O2 + 2H2O = 2Fe2++ 4OH—
2Fe + O2 + 2H2O = 2Fe(OH)2
Далее Fe(OH)2 переходит в Fe(OH)3
4Fe(OH)2 + O2 + 2H2O = Fe(OH)3
В азотной кислоте
А: Fe – 2e— = Fe2+
K: 2H+ + NO3— + e— = NO2 + H2O
Fe + 4H+ + 2NO3— = Fe2++ 2NO2 + 2H2O
Fe + 4HNO3 = Fe(NO3)2 + 2NO2 + 2H2O
3)при ну: V(N₂) = n(N₂)*22,4=N(N₂)/N[a](N₂)*22,4=(9*10²³/6.022*1023)*22,4≈33,6 литра
4)решение возможно, только если вещество - газ; при ну: n = V/V[m] = 16,8/22,4 = 0,75 моль
5)m(O₂) = n(O₂)*M(O₂)=V(O₂)*M(O₂)/22,4 = 5,8*32/22,4≈8,3 грамм